大肠杆菌细胞壁衍生的碳点抑制脓毒症细胞因子风暴
期刊:Advance materials
作者:Yinan Li
分区:中科院一区
影响因子:26.8
一、文章概述
该研究围绕脓毒症中“细胞因子风暴”核心机制,创新性地提出并验证了一种以病原体衍生碳点作为治疗手段的策略。以大肠杆菌细胞壁为原料制备碳点(E-CDs),系统评估其在细胞、脓毒症小鼠模型、非人灵长类模型以及患者来源细胞中的抗炎和免疫调控作用,揭示其通过多通路协同抑制先天免疫过度激活,从而缓解脓毒症进程。
二、研究背景
脓毒症通常由感染引发失控免疫反应,即宿主先天免疫系统的过度激活。革兰阴性菌及其脂多糖(LPS)通过TLR4通路触发NF-κB介导的炎症级联反应,同时炎症诱导的线粒体损伤和mtDNA释放又进一步激活cGAS–STING通路,加剧炎症。碳点因其良好的生物相容性和可调控生物活性,被认为具有潜在治疗价值,但其在脓毒症免疫调控中的系统研究仍十分有限。本文作者通过大肠杆菌细胞壁来源碳点,探究其在脓毒症治疗和机制通路中的作用。
三、研究结果
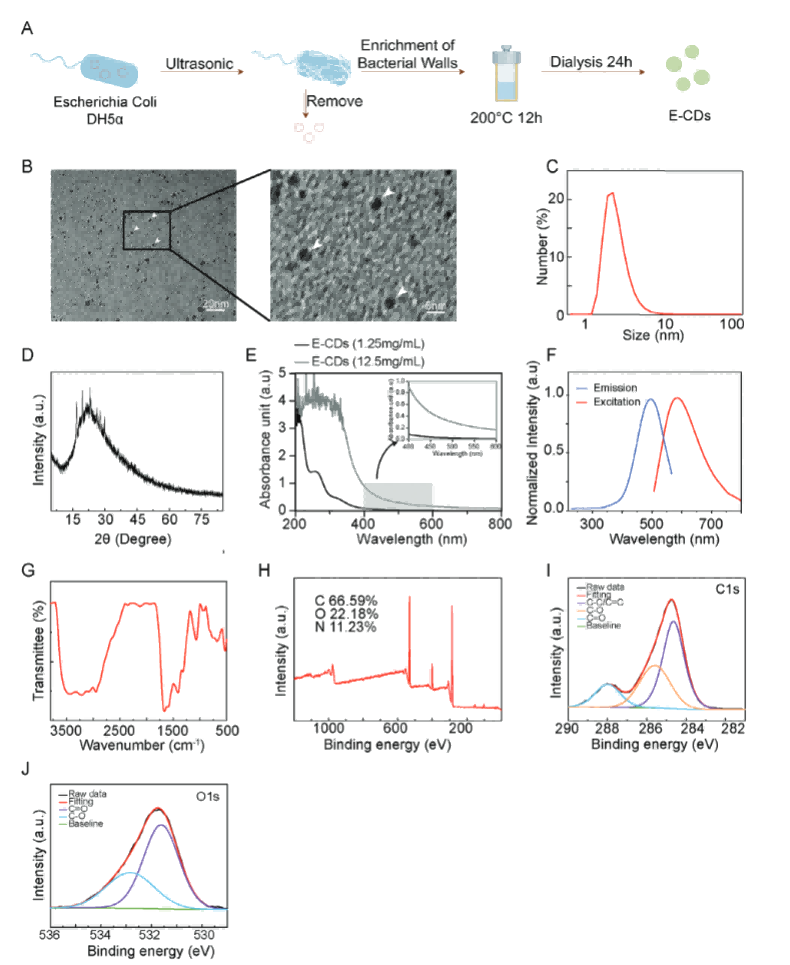
通过大肠杆菌细胞壁制备碳点,扫描电镜和DLS(动态光散射)表明制备出的碳点具有纳米尺度的结构。XRD、紫外吸收光谱、荧光光谱进一步证实结构和组成。FT-IR和XPS表征其表面含有丰富的C-O、C=O官能团,为其后续多种生物功能奠定基础。
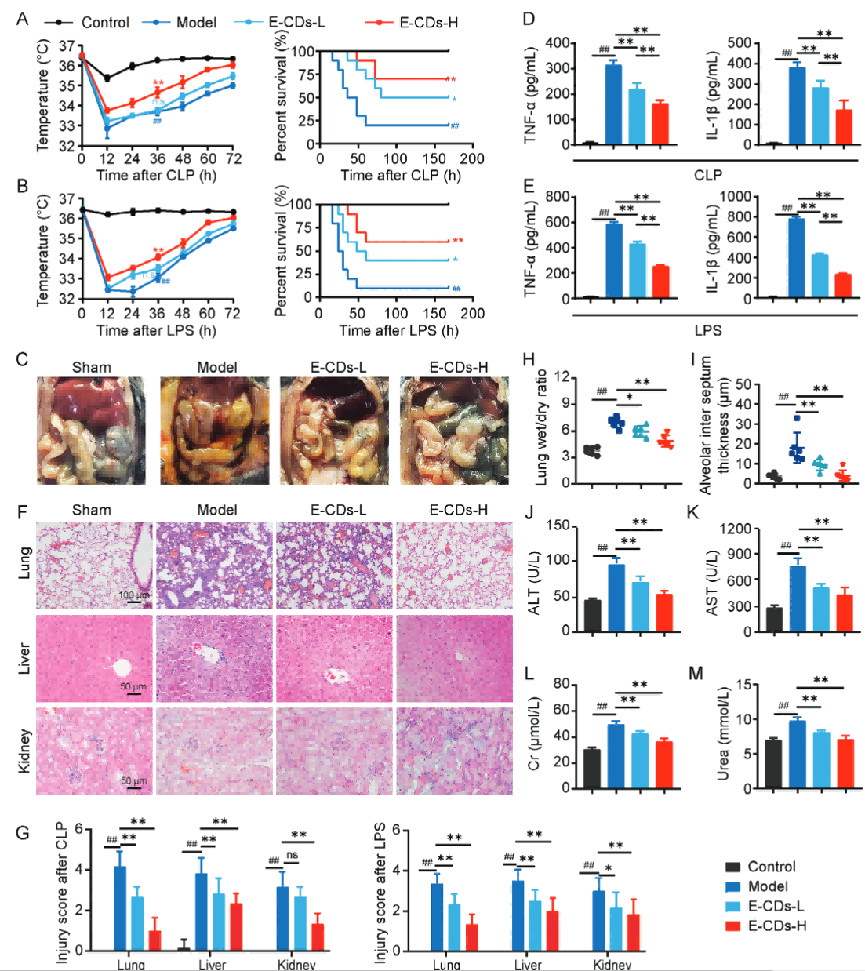
CLP和LPS两种造模方式,低剂量和高剂量的E-CDs,监测小鼠体温和生存率,造模组相比于对照明显体温升高,存活率降低,而E-CDs的干预改善了体温,提高了生存率,且具有剂量依赖性。ELISA测量血清中炎症因子的水平,也观察到E-CDs组有明显的降低。
干预组小鼠腹腔的肿胀和炎症感染情况相比于模型组也较轻。HE染色显示模型组肝索结构紊乱,伴有多种弥漫性凝固,肾小球肿胀和肾小管上皮细胞空泡化。相比之下,E-CDs治疗组显示出肺、肝和肾损伤的显著改善,肺部干重、肺泡厚度、不同器官的损伤指标(肌酐、尿素、ALT、AST等)和损伤评分也支持上述结论。
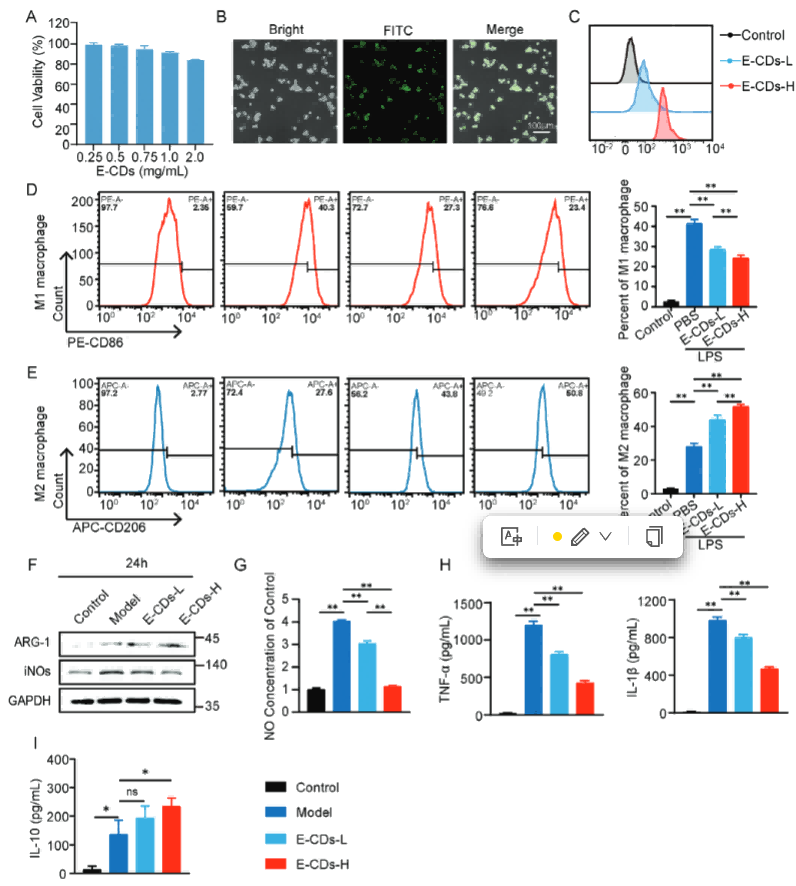
通过荧光标记E-CDs,观察到巨噬细胞内吞了大部分E-CDs。流式检测,内吞后E-CDs明显促进LPS刺激的巨噬细胞从促炎的M1型改为抗炎的M2型极化,WB检测M1和M2的标志物同样支持这一结论。定向极化后,在E-CDs的影响下,NO和炎症因子的分泌也相比于LPS组明显降低,抗炎的IL-10则显著升高。
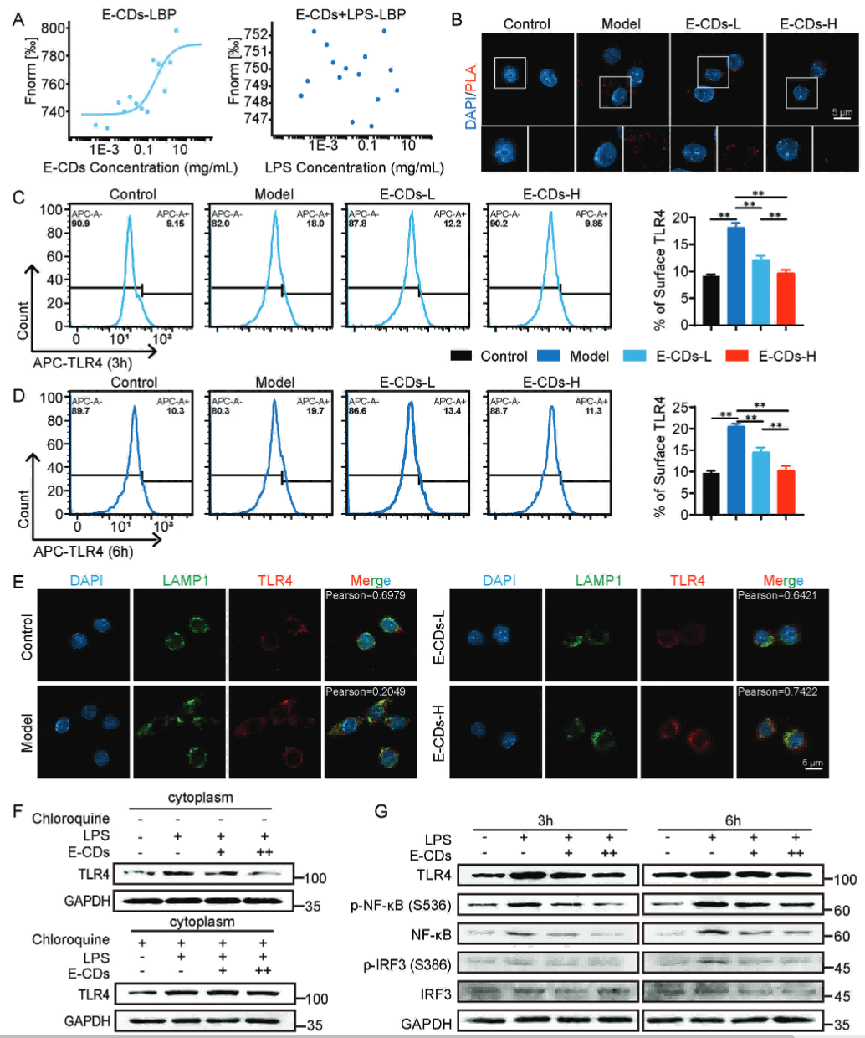
微量热泳动证实E-CDs和LBP的结合,同时其可以干扰LPS与LBP的结合。PLA实验证明,LPS-LBP在巨噬细胞中存在明显的共定位,而加入E-CDs后,共定位信号显著减少。流式显示膜表面TLR4的表达量随E-CDs剂量依赖性下降。
通过共聚焦,发现干预组TLR4和溶酶体的Pearson相关系数显著增加,证实E-CDs(具有溶酶体亲和性)降低TLR4表达是通过促进其转运至溶酶体降解实现的。溶酶体抑制剂氯喹处理后,TLR4不再随着E-CDs的干预而降低表达也证实了这一点。进一步研究TLR4下游信号通路,NF-kB和IRF3表达升高并磷酸化,核转位,促进炎症因子的分泌增加。
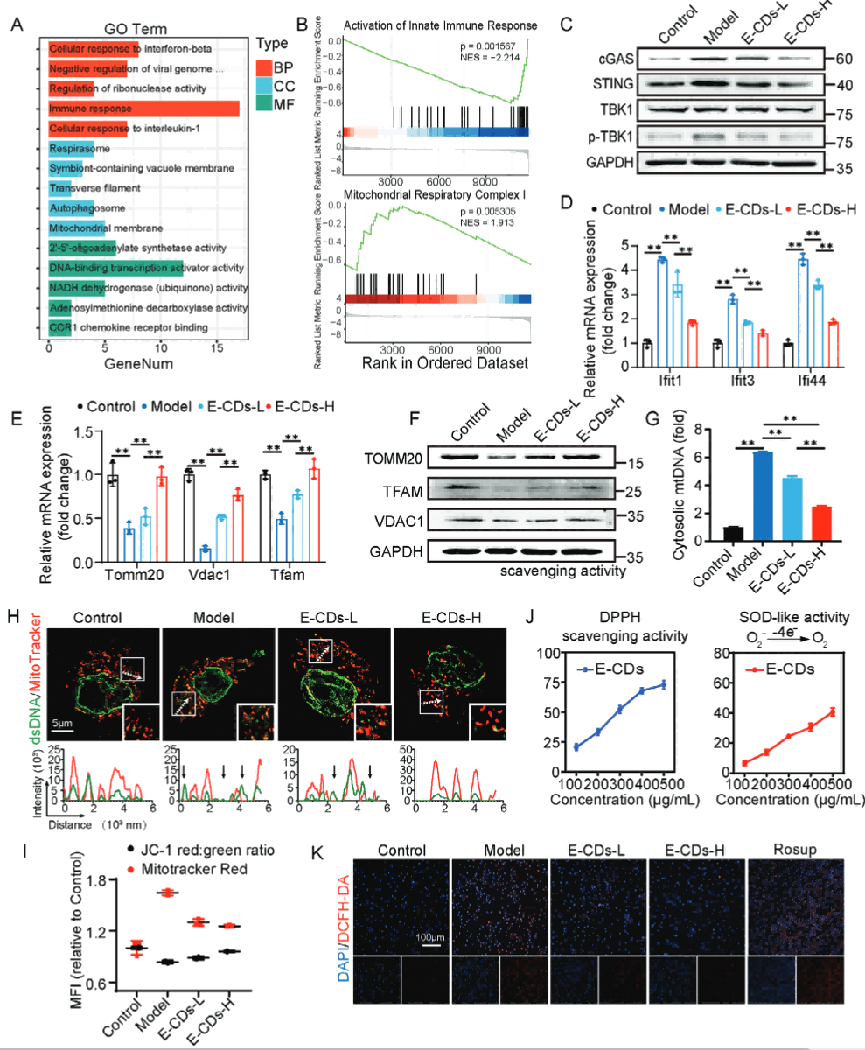
GO分析显示,E-CDs显著调节巨噬细胞免疫反应的生理过程,也包括炎症条件下线粒体膜和线粒体呼吸等分子功能的影响。GSEA证实E-CDs降低先天免疫过度激活相关基因的表达,同时提高了线粒体呼吸链复合物1相关基因表达,提示E-CDs可能具有提高线粒体功能的作用。根据KEGG提示,进一步研究与DNA感受通路相关的cGAS、STING等,发现其表达也受E-CDs的抑制,同时影响了下游通路的磷酸化,与STING诱导炎症相关的干扰素基因也受到影响。
线粒体DNA作为DAMP,通过cGAS和STING通路与脓毒症密切相关。线粒体损伤实验返现,线粒体外膜转位酶20、电压依赖性阴离子通道1、线粒体DNA结合蛋白转录因子A,均在LPS刺激后升高,受到E-CDs干预后降低。
dsDNA抗体染色mtDNA,证实E-CDs能显著缓解LPS导致的线粒体DNA外漏。,JC-1和Mitotracker流式证明E-CDs缓解了LPS导致的线粒体质量增加和膜电位丧失。进一步探究机制,E-CDs通过抗氧化应激减轻线粒体DNA外漏,具有DPPH清除能力和SOD酶活性,能显著减少细胞被LPS刺激后的ROS水平,改善线粒体功能。
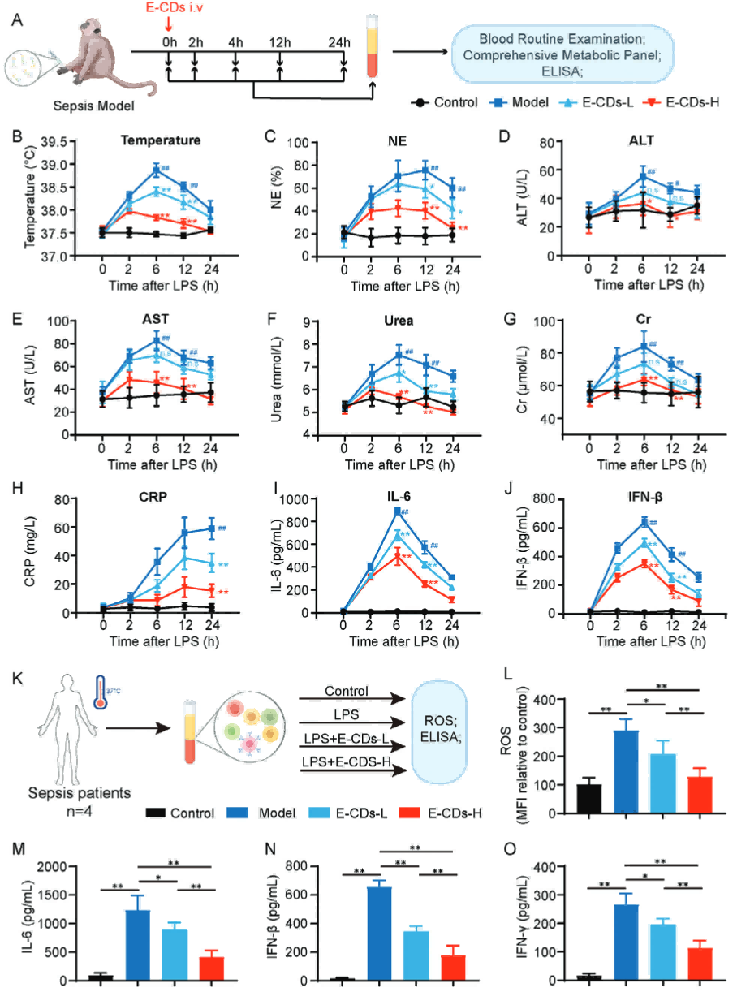
静脉注射E-CDs验证生物安全性,LPS注射食蟹猴诱导脓毒症,在2、6、12、24h分别检测各项指标的变化。包括体温、中性粒细胞百分比、C反应蛋白、ALT、AST、肌酐、尿素、炎症因子等。E-CDs均表现出显著的缓解炎症和治疗作用。
脓毒症患者血液分离PBMCs,刺激和干预后,检测ROS阳性细胞和炎症因子的分泌,同样表明E-CDs具有较好的抗炎抗氧化的功能。
四、研究结论
该研究证明,大肠杆菌细胞壁衍生碳点仍保留了细胞壁的部分功能,能够通过同时靶向TLR4-NF-κB和cGAS-STING两条关键免疫通路,协同抑制脓毒症中的细胞因子风暴,从而有效缓解系统性炎症反应和器官损伤,显示出良好的治疗潜力与转化前景。
五、创新与意义
本研究为脓毒症这一重大临床难题提供了全新的治疗思路,创新性的通过将病原体本身转化为治疗性纳米材料,展示了碳点在免疫调控和抗感染治疗中的巨大潜力。从材料制备、分子机制到非人灵长类和患者细胞验证,形成完整的研究思路。也为其他感染性疾病及炎症相关疾病的纳米药物设计提供了重要理论依据和技术范式。
文献原文:


