小肠γδT17细胞通过STING/ C1q诱导的小胶质突触修建促进雄性小鼠SAE
作者:Yuming Wu, Yujing Zhang, Yuan Yu等
doi:https://doi.org/10.1038/s41467-025-62181-3

文章概述
本研究首次揭示,脓毒症可诱导小肠来源的特定免疫细胞亚群——IL-7Rhigh CD8low γδ T17细胞——向脑膜迁移,进而通过分泌IL-17A激活脑内小胶质细胞,引发cGAS-STING-C1q信号通路的级联反应,最终导致海马区兴奋性突触的过度修剪,造成认知功能障碍。研究同时提出并验证了4-辛基衣康酸(4-OI) 作为一种潜在治疗剂,通过双重机制(抑制γδ T17细胞迁移和促进STING蛋白降解)有效缓解SAE。
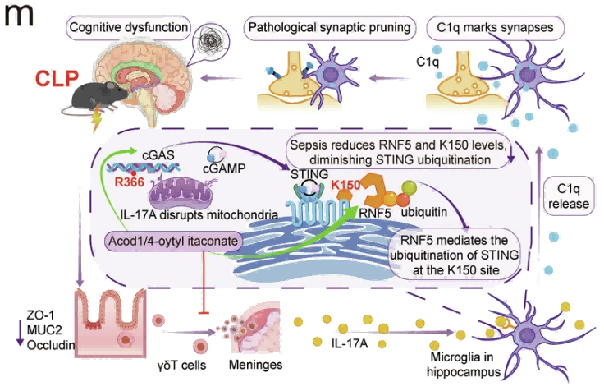
研究背景
1.脓毒症相关脑病(SAE)的严重性与未解问题:
脓毒症是一种全球性高死亡率疾病,SAE是其严重并发症,以神经功能障碍为特征,显著增加ICU患者死亡率。
尽管SAE常被认为是可逆的,但约40%的患者会出现长期神经症状,如记忆障碍、抑郁、焦虑等,目前尚缺乏有效的治疗策略,机制也未完全阐明。
2.“肠源脓毒症”与“脑-肠轴”的概念:
肠道被认为是驱动脓毒症和多器官功能障碍的“引擎”,即“肠源脓毒症”。
肠道富含免疫细胞,特别是γδ T细胞和Th17细胞,它们维持黏膜免疫平衡和屏障完整性。
3.已知但未解的机制:
已有研究表明,肠道免疫细胞(如γδ T17细胞)在脓毒症后可迁移至肺部加重急性肺损伤。
另有研究提示,γδ T17细胞可能迁移至脑膜并分泌IL-17A,影响神经炎症和认知功能。
小胶质细胞介导的突触修剪(尤其是依赖补体C1q的修剪)与SAE的认知障碍相关,但上游调控机制不清楚。
研究结果
小肠来源的IL-7RhighCD8lowγδ T17细胞在脓毒症后迁移至脑膜并加重SAE。
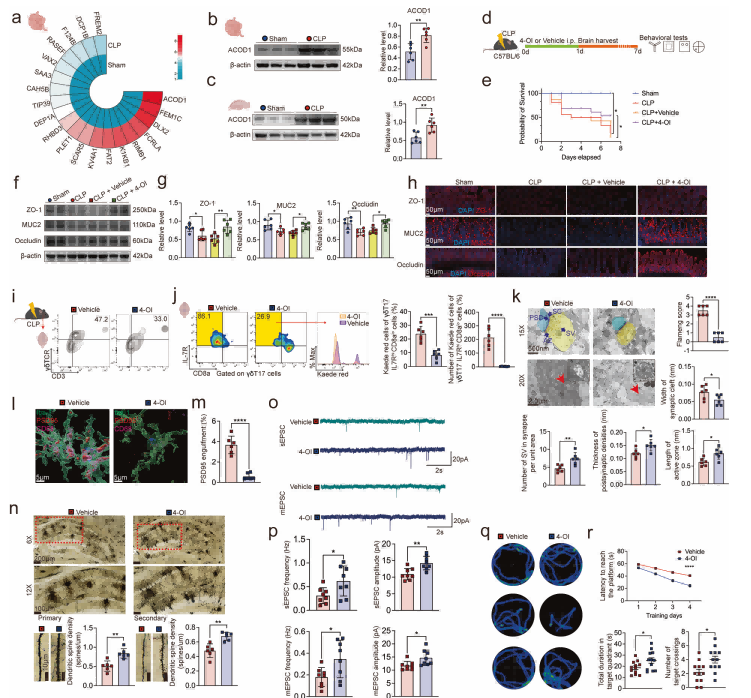
通过流式细胞术分析发现:CLP后,小肠γδ T细胞减少,脑膜γδ T细胞增加,且超过50%为分泌IL-17A的γδ T17细胞。利用Kaede小鼠的光转换实验证实,脑膜中大多数IL-7R^high CD8^low γδ T17细胞来源于小肠。在γδT细胞中条件性敲除IL-17A(Trdc^CreERT2; Il17a^flox/flox)可显著减轻CLP诱导的突触丢失、线粒体损伤和认知功能障碍。

IL-17A损害线粒体并激活cGAS-STING-C1q通路。
IL-17A处理BV2细胞后,观察到线粒体膜电位下降、线粒体肿胀,并释放mtDNA触发cGAS-STING通路。IL-17A处理或与γδ T细胞共培养后,BV2细胞内cGAS、STING和C1q蛋白表达上调;敲低γδ T细胞的IL-17A可减少小胶质细胞线粒体损伤,降低cGAS、STING、C1q水平。在海马区过表达IL-17A上调cGAS、STING和C1q,并降低突触蛋白PSD95/SYN;而在IL-17A条件敲除小鼠中,这些变化被抑制。
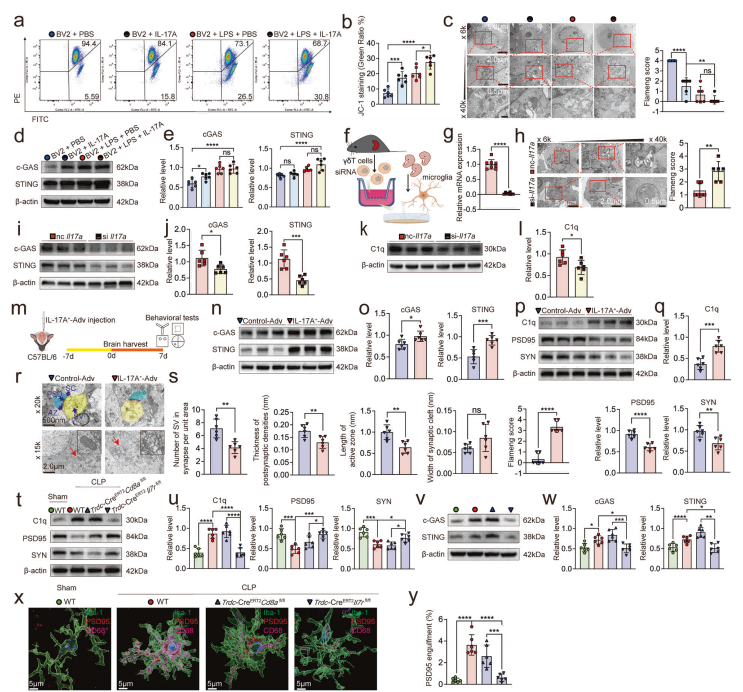
抑制STING或C1q可逆转突触修剪和认知障碍。
使用STING抑制剂H151处理可减少C1q表达,增加PSD95和突触素表达,缓解突触修剪,从而改善认知结果。H151还逆转了cGAS过表达在小胶质细胞中引起的突触损伤。直接中和C1q可减少小胶质细胞对突触蛋白的吞噬,改善认知并恢复突触完整性。
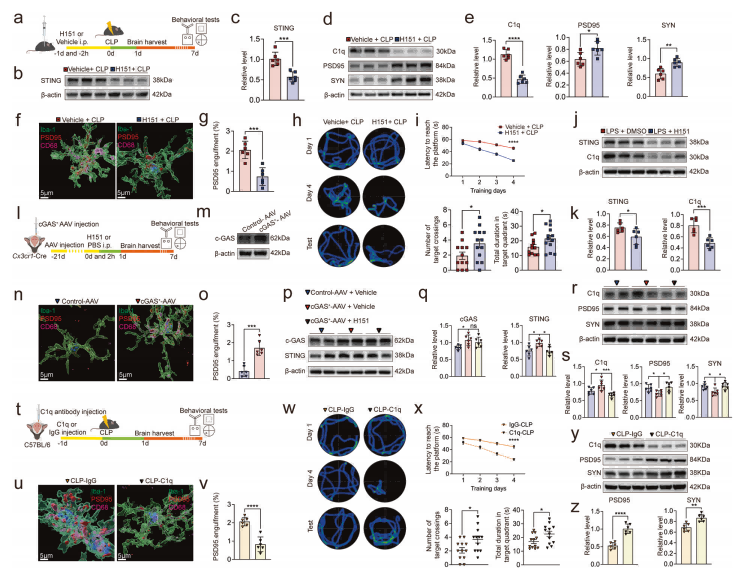
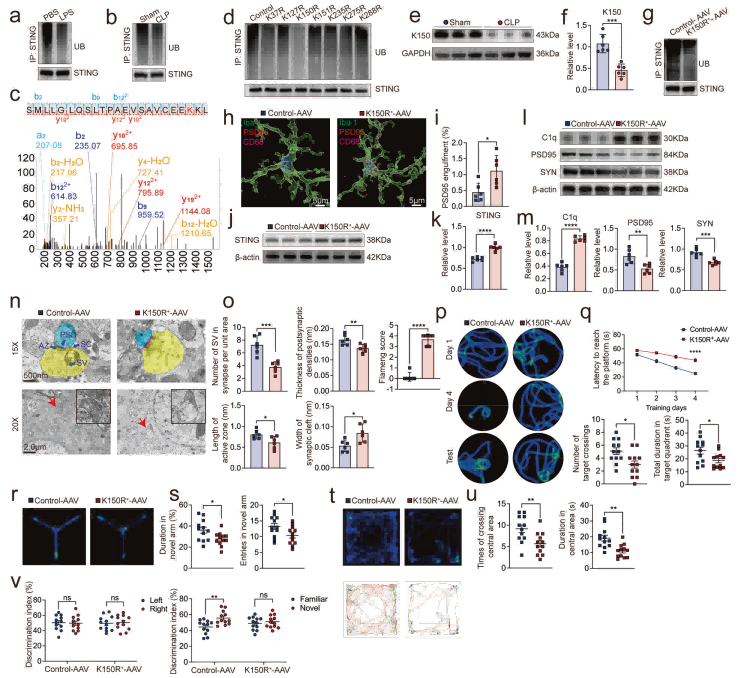
STING的K150位点泛素化是调控其稳定性和SAE严重程度的关键。
脓毒症后,小胶质细胞中STING的泛素化水平降低,特别是K150位点的泛素化。K150R突变导致STING累积、C1q上调、突触修剪加剧和认知功能恶化。E3泛素连接酶RNF5被鉴定为负责STING K150位点泛素化的关键酶,脓毒症后其与STING的相互作用减弱。
4-OI通过双重机制有效缓解SAE。
机制一(外周):抑制小肠IL-7R^high CD8^low γδ T17细胞向脑膜的迁移,降低脑膜和脑内IL-17A水平。
机制二(中枢):穿透血脑屏障,直接作用于小胶质细胞,促进STING的K150位点泛素化(通过上调RNF5),加速STING降解,从而抑制cGAS-STING-C1q通路。
效果:4-OI治疗显著改善脓毒症小鼠的突触结构、线粒体功能、海马神经传递效率以及多种行为学测试中的认知表现。
内源性衣康酸合成酶ACOD1具有保护作用。
Acod1^-/-小鼠在CLP后死亡率极高,存活者表现出更严重的突触损伤、小胶质细胞激活和认知障碍。在小胶质细胞中敲低Acod1基因,会加剧脓毒症引起的cGAS-STING通路激活、C1q上调、突触吞噬和结构损伤。Acod1敲低同样会减少STING的K150泛素化。
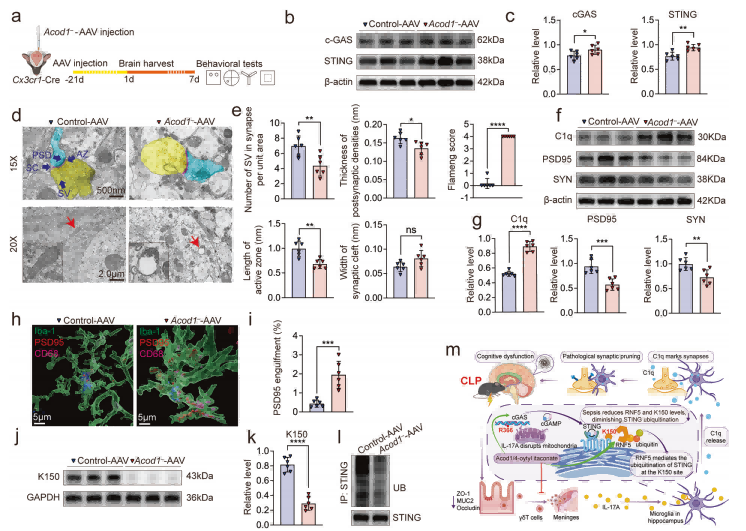
研究结论、意义
研究结论:本研究揭示了一条全新的SAE发病机制轴:脓毒症 → 小肠屏障破坏 → IL-7R^high CD8^low γδ T17细胞迁移至脑膜 → 分泌IL-17A → 小胶质细胞线粒体损伤 → mtDNA释放 → cGAS-STING通路激活 → STING K150泛素化抑制 → STING累积 → C1q上调 → 小胶质细胞介导的异常突触修剪 → 海马认知功能障碍。
研究的创新性:跨器官系统研究:成功整合了免疫学(肠道T细胞)、神经科学(小胶质细胞、突触)和代谢学(衣康酸)的研究方法,为研究其他系统性疾病(如自身免疫病、神经退行性疾病)的全身性影响提供了范式。
研究意义:提出新的治疗靶点:针对γδ T17细胞迁移、STING蛋白稳定性或C1q功能的药物可能成为治疗SAE的新方向。验证4-OI的治疗潜力:4-OI作为一种能穿透血脑屏障的免疫代谢物衍生物,展现出多靶点、多环节的治疗优势,具有较高的临床转化前景。提供生物标志物思路:脑膜或脑脊液中IL-7R^high CD8^low γδ T17细胞、STING泛素化水平或C1q浓度,可能作为SAE诊断或预后评估的潜在标志物。
文献原文:


