目前临床治疗,如抗感染、液体复苏、器官支持等,虽可缓解症状,却难以有效修复肠屏障功能。因此,研发一种能同时控制炎症、保护肠道上皮的新策略至关重要。
肠道靶向解码工程化胶囊通过广谱抗炎与抑制多聚ADP核糖聚合酶1依赖性细胞死亡(Parthanatos)机制防治脓毒症肠损伤
期刊:Advanced Science
分区:中科院一区
影响因子:14.1
一、研究背景
脓毒症(Sepsis)是一种由感染引发的系统性炎症综合征,其核心特征是免疫反应失衡与多器官功能障碍,其发病率及死亡率高。在脓毒症的病理过程中,肠道被视为“发动机器官”——其黏膜屏障受损、通透性升高、细菌移位等变化都会加重病情,导致继发性肠源性感染。
目前临床治疗,如抗感染、液体复苏、器官支持等,虽可缓解症状,却难以有效修复肠屏障功能。因此,研发一种能同时控制炎症、保护肠道上皮的新策略至关重要。
研究者同时关注到一种特殊的细胞程序性死亡形式——Parthanatos(PARP1过度激活所致的细胞死亡),其在神经退行性疾病等中已被证实参与病理进展,但其在脓毒症性肠损伤中的作用尚不明确。现有药物递送系统存在靶向性差、易被胃酸降解等问题,限制了肠损伤治疗药物的生物利用度。
奥拉帕利(OLA)是一种 PARP-1 抑制剂,已有肿瘤领域应用基础,因此成为候选药物。
二、主要研究内容
l 设计并制备新型纳米药物递送系统 cp-OLA@MΦNPs,核心为包裹奥拉帕利的 PLGA 纳米粒,表面包覆巨噬细胞膜,外层封装 pH 响应型 EUDRAGIT L 30 D-55 胶囊。
l 验证该系统的理化特性、pH 响应释放能力及肠道靶向性。
l 体外实验评估其对肠上皮细胞(IEC-6)的保护作用,包括抑制 Parthanatos、减轻氧化损伤、修复紧密连接功能。
l 体内实验在脓毒症小鼠模型中,检测其抗炎效果、肠屏障保护作用、多器官损伤修复及生存率提升情况。
l 系统评估该纳米药物的生物安全性,包括细胞毒性、溶血活性及体内器官毒性。
三、研究思路与技术路线
研究思路
本研究围绕脓毒症中肠屏障损伤的关键机制——炎症风暴与细胞程序性死亡(parthanatos)展开。研究团队设计了由奥拉帕利(PARP1抑制剂)封装于PLGA核内、外层包裹巨噬细胞膜的仿生纳米颗粒,再通过pH响应肠溶胶囊实现靶向肠道递送。通过“体外细胞—体内动物—机制层面”三维验证体系,逐层证实疗效与作用机制。整体思路实现了从“病理机制识别→仿生载体构建→靶向递送验证→系统疗效评估”的闭环研究路径 。
技术路线
1.材料制备:通过纳米沉淀法制备包裹奥拉帕利的 PLGA 纳米粒(OLA@NPs),经共挤出法包覆巨噬细胞膜得到 OLA@MΦNPs,冻干后封装于 gelatin 胶囊并包覆 EUDRAGIT L 30 D-55,获得 cp-OLA@MΦNPs。
2.表征检测:通过动态光散射、透射电镜、SDS-PAGE、Western blot 等验证纳米粒尺寸、结构、蛋白组成及细胞因子结合能力;通过模拟胃肠液实验和动物活体成像验证 pH 响应释放及肠道靶向性。
3.体外实验:用 H₂O₂诱导 IEC-6 细胞氧化损伤模型,通过 CCK-8、流式细胞术、彗星实验、免疫荧光等检测细胞活力、凋亡率、DNA 损伤及紧密连接蛋白(ZO-1、E-cadherin)表达。
4.体内实验:通过腹腔注射 LPS 建立小鼠脓毒症模型,分组给予空胶囊、游离 OLA、OLA@MΦNPs、cp-OLA@MΦNPs 治疗,检测血清细胞因子、肠屏障功能标志物、器官病理变化及生存率。
5.安全性评估:在 HUVEC、L929、IEC-6 细胞中检测细胞毒性;通过红细胞孵育实验检测溶血活性;在健康小鼠中检测血液学指标、生化标志物及器官病理切片。
四、研究结果
1.理化特性与靶向性
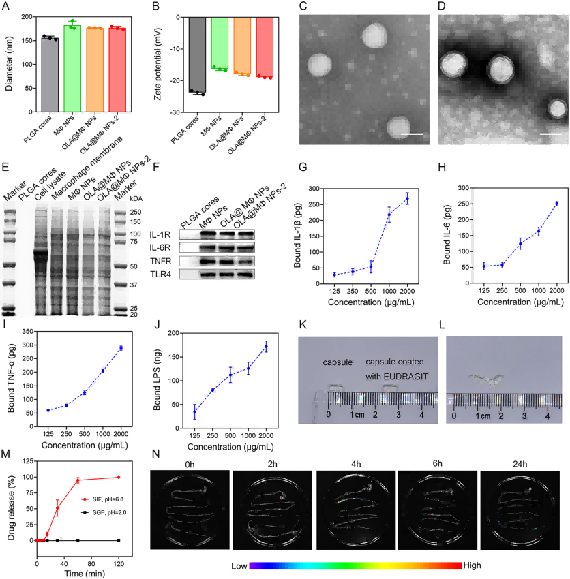
纳米粒结构与蛋白组成验证:动态光散射结果显示,PLGA 核心、MΦNPs、OLA@MΦNPs 及 cp-OLA@MΦNPs(从胶囊中分离)的水动力直径分别为 155.75 nm、182.48 nm、176.63 nm、176.70 nm,zeta 电位为 -16.23 ~ -18.81 mV,证明冻干和封装过程对纳米粒结构影响极小;透射电镜(TEM)观察到 cp-OLA@MΦNPs 具有典型核壳结构,与裸 PLGA 核心存在显著差异;SDS-PAGE 和 Western blot 分析显示,cp-OLA@MΦNPs 保留巨噬细胞膜关键蛋白受体(IL-1R、IL-6R、TNFR、TLR4),蛋白谱与纯巨噬细胞膜一致,且不含胞内蛋白(图 1A-F)。细胞因子与 LPS 结合能力:将 OLA@MΦNPs 与 IL-1β、IL-6、TNF-α 及 LPS 共孵育,结果显示纳米粒可剂量依赖性结合上述炎症介质,且结合效率随浓度升高而提升(图 1G-J)。pH 响应释放与肠道靶向性:胶囊在模拟胃液(pH=2.0)中 120 分钟内药物释放量极低,而在模拟肠液(pH=6.8)中 60 分钟内释放率超 90%,120 分钟完全释放;DiR 荧光标记的 cp-OLA@MΦNPs 口服后,2 小时主要集中在胃内,4 小时后在肠道广泛分布,证实其肠道靶向释放特性。
2.OLA@MΦNPs 对肠上皮细胞 Parthanatos 的抑制作用
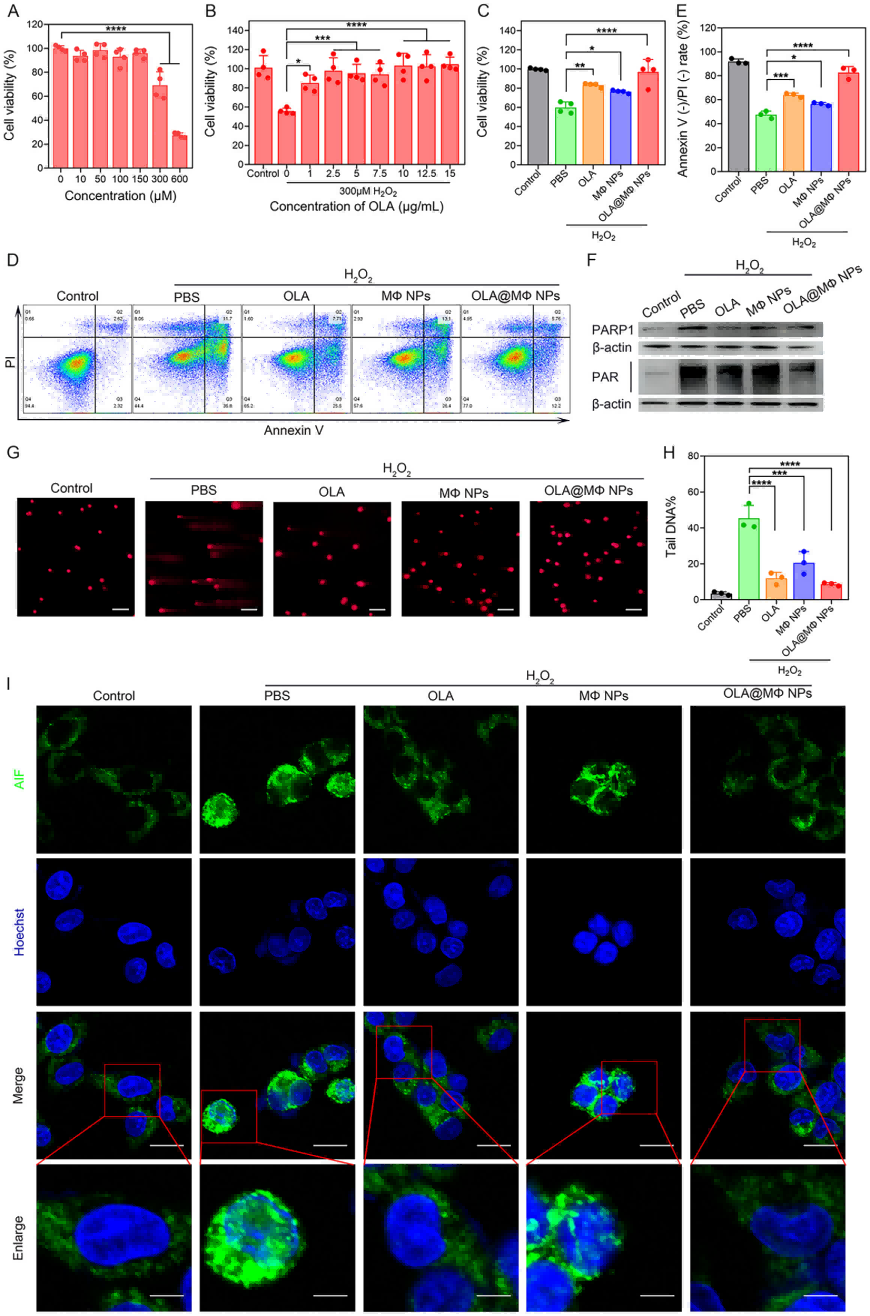
细胞活力与凋亡改善:CCK-8 实验显示,300 μM H₂O₂ 可显著降低 IEC-6 细胞活力,而 5 μg/mL OLA 或等效 OLA@MΦNPs 可显著提升细胞活力;流式细胞术(Annexin V/PI 染色)证实 OLA@MΦNPs 可减少 H₂O₂ 诱导的细胞凋亡(图 2A-E)。Parthanatos 相关分子调控:Western blot 结果显示,H₂O₂ 处理后 IEC-6 细胞 PARP1 和 PAR 表达显著升高,而 OLA 或 OLA@MΦNPs 处理可显著下调二者水平;彗星实验表明,OLA@MΦNPs 可减轻 H₂O₂ 诱导的 DNA 损伤;免疫荧光显示,OLA@MΦNPs 可抑制 AIF 核转位,减少 chromatin 浓缩和 DNA 片段化(图 2F-I)。
3. OLA@MΦNPs 对肠上皮损伤与屏障通透性的改善
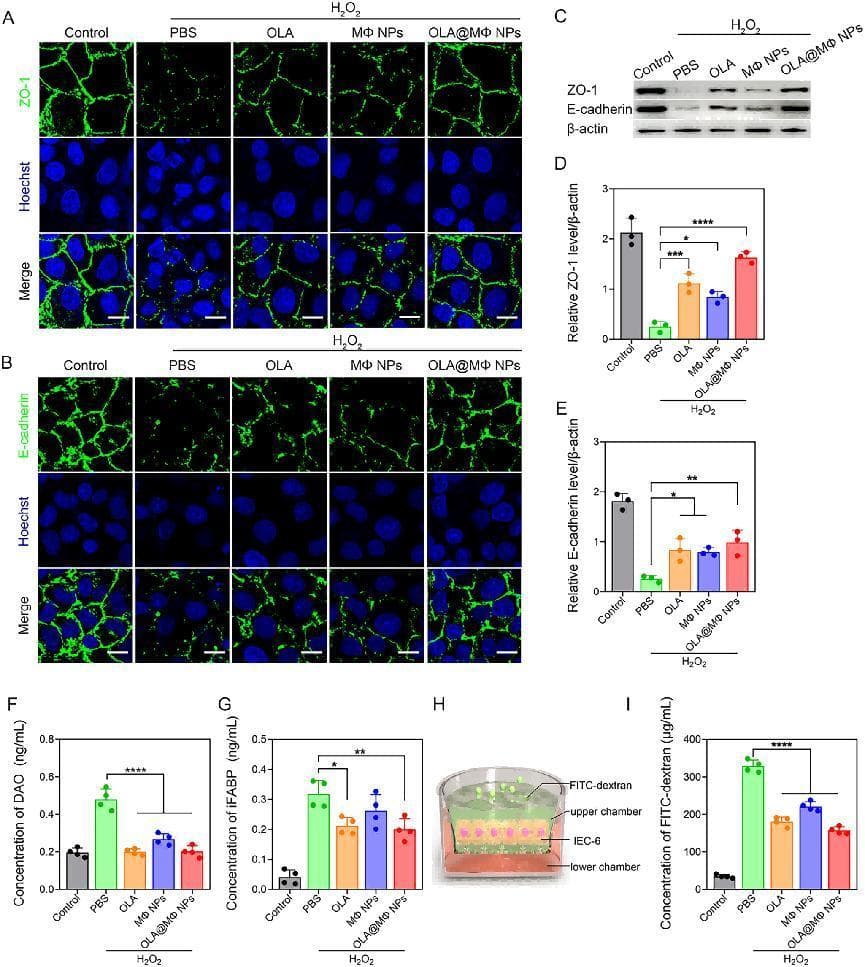
紧密连接蛋白表达恢复:免疫荧光显示,H₂O₂ 刺激导致 IEC-6 细胞 ZO-1 和 E-cadherin 表达减少且分布不连续,而 OLA@MΦNPs 处理可恢复二者连续线性分布;Western blot 进一步证实,OLA@MΦNPs 组 ZO-1 和 E-cadherin 表达水平显著高于 OLA 组和 MΦNPs 组(图 3A-E)。肠损伤标志物与通透性降低:H₂O₂ 处理后,IEC-6 细胞上清中 DAO 和 iFABP 水平显著升高,而 OLA@MΦNPs 处理可显著降低二者浓度;Transwell 实验显示,OLA@MΦNPs 组下室 FITC - 葡聚糖浓度较 PBS 组降低 52.13%,屏障通透性改善效果最优(图 3F-I)。
4.cp-OLA@MΦNPs 对脓毒症小鼠的体内治疗效果
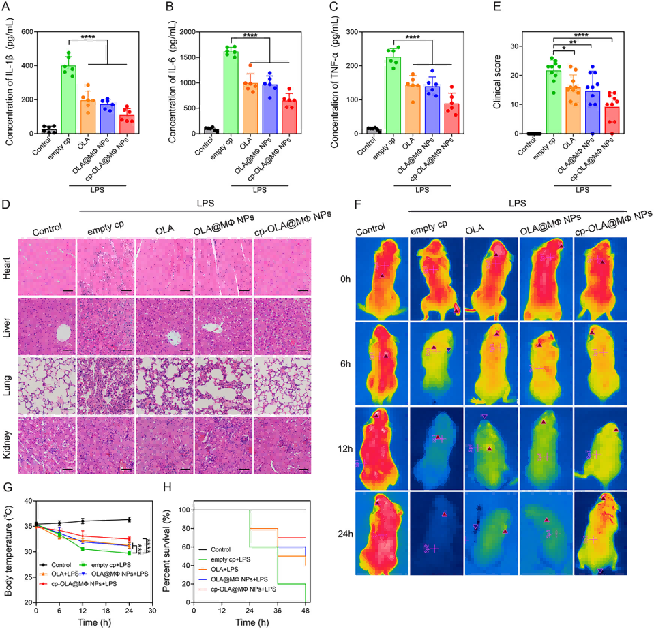
炎症因子抑制与器官保护:LPS 诱导脓毒症后,小鼠血清 IL-1β、IL-6、TNF-α 水平显著升高,而 cp-OLA@MΦNPs 处理可显著降低三者浓度,且效果优于游离 OLA 和 OLA@MΦNPs;HE 染色显示,cp-OLA@MΦNPs 组小鼠肺、肝、肾等器官的炎症细胞浸润显著减少,组织损伤修复最明显(图 4A-D)。临床症状与生存率改善:cp-OLA@MΦNPs 处理可显著降低脓毒症小鼠临床评分,缓解 LPS 诱导的体温下降;生存曲线显示,空胶囊组 48 小时生存率为 0%,而 cp-OLA@MΦNPs 组生存率提升至 70%,显著高于 OLA 组(40%)和 OLA@MΦNPs 组(50%)(图 4E-H)
5.cp-OLA@MΦNPs 对脓毒症小鼠肠损伤的保护作用
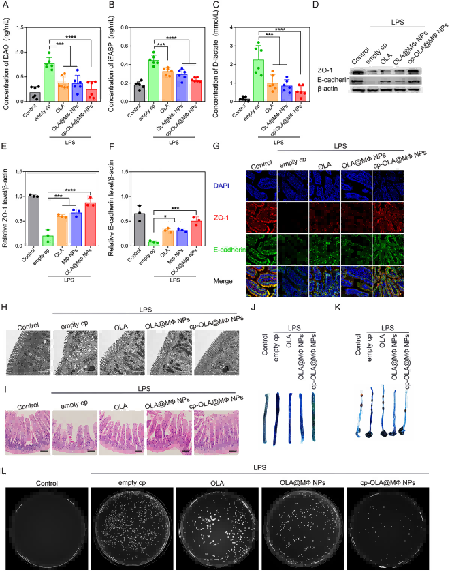
肠屏障功能标志物下调:脓毒症小鼠血清 DAO、iFABP、D - 乳酸水平显著升高,cp-OLA@MΦNPs 处理可显著降低三者浓度,且效果优于其他治疗组,提示肠道屏障损伤减轻(图 5A-C)。肠道结构与超微结构修复:Western blot 和免疫荧光显示,cp-OLA@MΦNPs 组小鼠肠道 ZO-1 和 E-cadherin 表达显著上调;TEM 观察到,该组小鼠肠道微绒毛排列整齐,细胞间隙狭窄,线粒体结构完整,而空胶囊组微绒毛稀疏紊乱、线粒体肿胀破裂;HE 染色显示,cp-OLA@MΦNPs 组肠道绒毛长度增加、结构完整,黏膜上皮脱落和上皮下间隙扩张现象显著改善(图 5D-I)。细菌易位减少:Evans 蓝渗漏实验显示,cp-OLA@MΦNPs 组小鼠肠道 Evans 蓝渗漏量显著降低;腹腔灌洗液细菌培养结果显示,该组细菌菌落数显著少于其他治疗组,证明肠道屏障完整性恢复可减少细菌易位(图 5J-L)。
6.cp-OLA@MΦNPs 的生物安全性
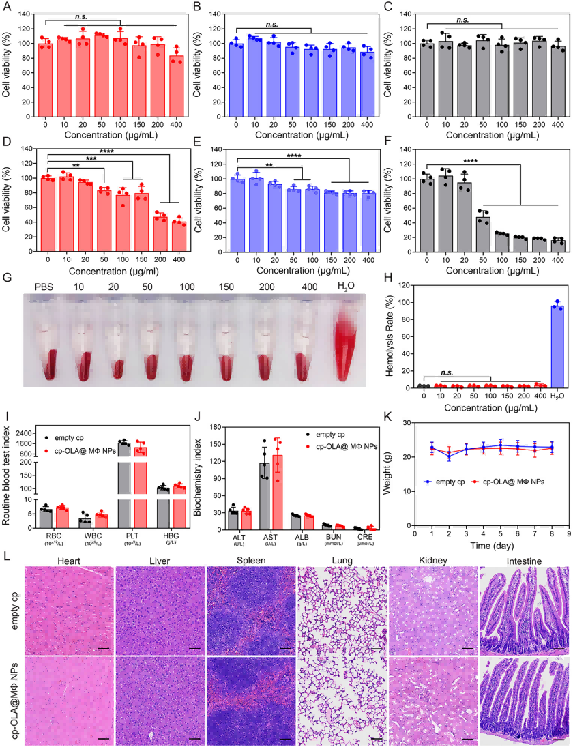
体外细胞毒性低:CCK-8 实验显示,OLA@MΦNPs 浓度高达 400 μg/mL 时,对 HUVEC、L929、IEC-6 细胞活力无显著影响,而游离 OLA 在 50 μg/mL 时即显著降低细胞活力;溶血实验显示,OLA@MΦNPs 与小鼠红细胞共孵育 24 小时无溶血现象(图 6A-H)。体内安全性良好:健康小鼠口服 cp-OLA@MΦNPs(等效 10 mg/kg OLA)后,48 小时内血常规(RBC、WBC、PLT、HBG)和血生化指标(ALB、ALT、AST、BUN、CRE)无显著异常,体重稳定;HE 染色显示,心、肝、脾、肺、肾、肠道等器官无组织损伤(图 6I-L)。
五、研究结论
该研究成功构建了兼具 pH 响应靶向递送、广谱抗炎和 Parthanatos 抑制功能的工程胶囊 cp-OLA@MΦNPs。该胶囊可耐受胃酸,在肠道精准释放药物,通过巨噬细胞膜受体中和炎症因子,奥拉帕利抑制肠上皮细胞 Parthanatos,双重机制保护肠屏障。体内外实验证实其能有效减轻脓毒症相关肠损伤,降低细菌易位,缓解多器官炎症,显著提升脓毒症小鼠生存率。cp-OLA@MΦNPs 生物安全性良好,为脓毒症治疗提供了安全有效的新型靶向策略,为脓毒症肠损伤治疗提供了新型纳米药物平台,具有临床转化潜力。
六、创新与局限性
创新性:
l 首次明确 Parthanatos 在脓毒症肠损伤中的关键作用,提出 “抗炎 + 抑制程序性坏死” 双重靶向治疗策略。
l 融合巨噬细胞膜的天然抗炎特性与 pH 响应型胶囊的靶向递送功能,实现药物肠道局部精准释放,提升生物利用度。
l 体内外结合、分子至整体病理层面全面论证,实现了多层次验证体系。
局限性
l 机制深度不足,对信号通路调控的下游机制探讨有限。
l 未深入探讨药物在肠道内的代谢过程及长期安全性,且未明确最佳给药剂量和给药时机。
l 巨噬细胞膜来源可能存在个体差异,提取与规模化制备成本较高,临床转化仍需进一步研究。
七、启发
1.提供了药物与生物膜结合的新方向,提升治疗精准度,可推广至其他炎症性疾病;
2.Parthanatos 通路被证实为可靶向的新节点,有望成为炎症相关器官损伤的通用治疗靶点,为多种急性器官损伤的干预提供参考;
3.生物安全性是纳米药物临床转化的关键,天然生物膜包覆策略可降低纳米载体的免疫原性,为后续研发提供参考。
文献原文:


