功能性脂质纳米颗粒用于向革兰氏阴性菌安全递送大分子抗生素
期刊:Journal of Controlled Release
分区:中科院一区
影响因子:11.5
一、研究背景
抗菌耐药性(Antimicrobial Resistance, AMR)已成为全球公共卫生重大挑战。革兰阴性菌(如鲍曼不动杆菌、铜绿假单胞菌、大肠杆菌)因外膜结构致使多种抗生素难以穿透,其耐药性尤为突出。
多黏菌素B(Polymyxin B, PMB)是一种强效脂肽类抗生素,被视为“最后防线药物”。然而,由于其带正电、易与宿主细胞膜阴离子磷脂结合,造成肾毒性与神经毒性,严重限制了临床使用。
现有药物递送系统(如聚合物纳米粒、脂质体等)虽可缓释或改善药物分布,但存在制备复杂、规模化受限、靶向性不足等问题。
因此,研究者希望开发一种兼具高安全性与抗菌效率的PMB递送系统,突破其临床毒性瓶颈。
二、主要研究内容
本研究设计并制备了一种基于阴离子脂质的功能性脂质纳米颗粒(Lipid Nanoparticles, LNPs),用于包封并递送阳离子抗生素PMB。研究的主要内容包括:
设计与合成新型阴离子脂质C14-Glu₅,其含有寡谷氨酸阴离子头基和双C14烷基尾链,可通过静电作用与PMB形成复合物;
建立LNP自组装体系:利用乙醇/水两相快速混合制备PMB-LNP;
系统比较不同脂质(C14-Glu₅、C14-PS、C18-PS)与配比(1:4、4:1)下LNP性质、药物包封率与稳定性;
评估其体外抗菌性能、细胞毒性、血液相容性与体内药代动力学;
在中性粒细胞缺乏小鼠鲍曼不动杆菌感染模型中验证其治疗效果与安全性。
三、研究思路与技术路线
研究总体思路遵循“材料结构设计 → 递送体系构建 → 功能验证 → 机制探讨 → 体内转化评估”的逻辑。
材料设计思路
借鉴核酸LNP体系的电荷匹配设计理念,反向采用阴离子脂质来负载阳离子药物(PMB),实现电荷自组装。
C14-Glu₅ 通过寡谷氨酸结构与PMB形成稳定复合;
胆固醇与DSPC改善膜稳定性;
PEG脂质(ALC-0159)提升血液循环时间。
制备与表征方法
采用微流控混合技术获得粒径均一、结构稳定的LNP;
通过动态光散射(DLS)与TEM表征粒径、形貌;
利用HPLC测定药物包封率及释放曲线。
性能验证
体外:最小抑菌浓度(MIC)、最小杀菌浓度(MBC)、协同效应分析;
体内:药代动力学(半衰期、分布)与中性粒细胞缺乏小鼠感染模型疗效。
四、研究结果
1. PMB-LNPs的制备与表征
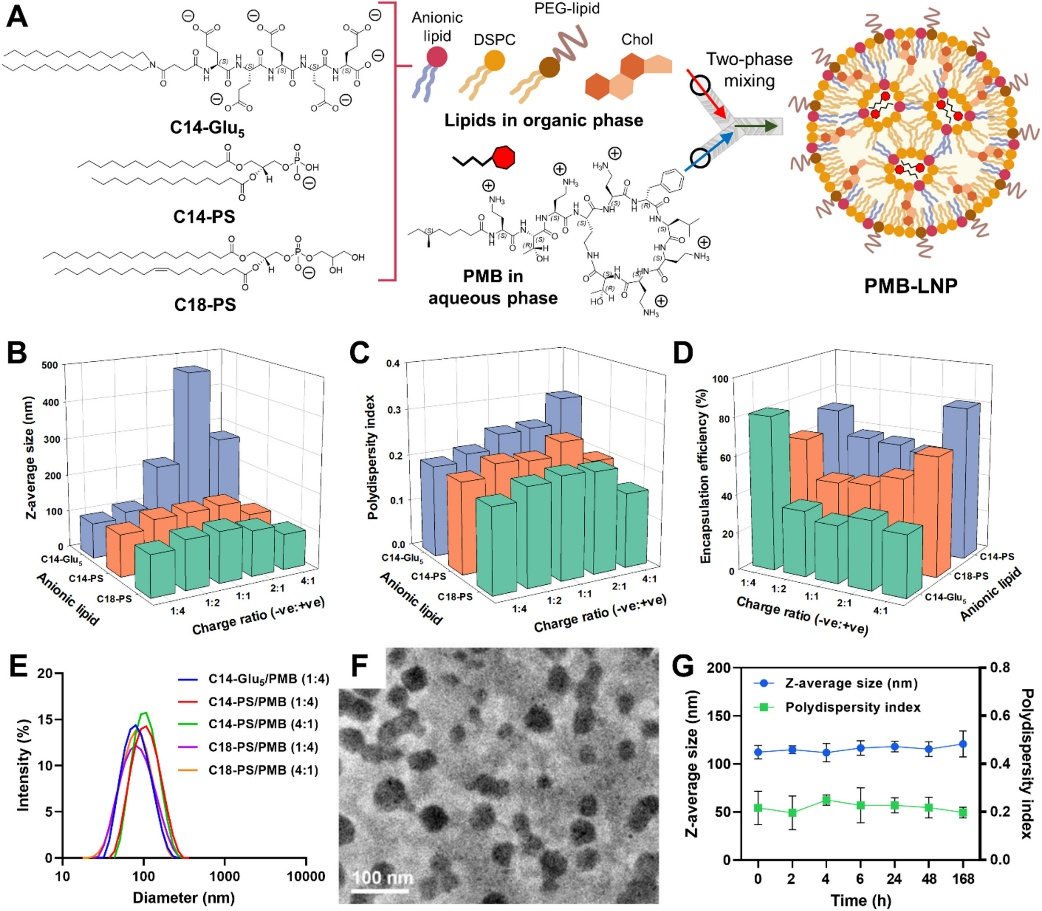
使用芴基甲氧羰基(Fmoc)化学通过固相技术合成了阴离子脂质C14-Glu5。为制备PMB-LNPs,将水相(PMB溶解在pH 7.4的磷酸盐缓冲盐水(PBS)中)与有机相(含有阴离子脂质(C14-Glu5或C14-PS或C18-PS)、胆固醇、DSPC和ALC-0159的乙醇溶液)快速混合(图1A)。当电荷比(-ve:+ve)从1:4增加到2:1时,C14-Glu5/PMB LNPs的Z-平均粒径逐渐从约94.5 nm增加到468.3 nm(图1B)。 电荷比进一步增加到4:1导致Z-平均粒径减小到约272.2 nm,同时多分散指数上升到0.3以上,表明异质性增加(图1C)。 在相同电荷比(1:1, 2:1 和 4:1)下,C14-PS(102.3 nm)和C18-PS(94.7 nm)产生的PMB-LNPs要小得多,这表明生成了更紧凑的PMB-脂质组装体。 在pH 7.4的生理PBS缓冲液中,所有PMB-LNPs均具有接近中性的zeta电位值。随后,基于它们的小尺寸(<120 nm)、低多分散指数(<0.2)和高达82%的高PMB包裹效率(图1D和S4),选择了五种最佳制剂(C14-Glu5/PMB (1:4);C14-PS/PMB (1:4) 和 (4:1);C18-PS/PMB (1:4) 和 (4:1))。这些制剂具有单分散的粒径分布,峰值直径为80-110 nm(图1E),在生理pH 7.4下表面带中性电荷。TEM图像(图1F)显示PMB-LNPs呈球形,内部具有电子致密的区域,表明结构上存在异质性。如图1G所示,所有优化的PMB-LNP制剂在含血清的PBS(pH 7.4)中于37℃下保持其Z-平均粒径和多分散指数长达168小时,证实了它们在生理环境下的出色稳定性。
3.2. 体外抗菌活性研究
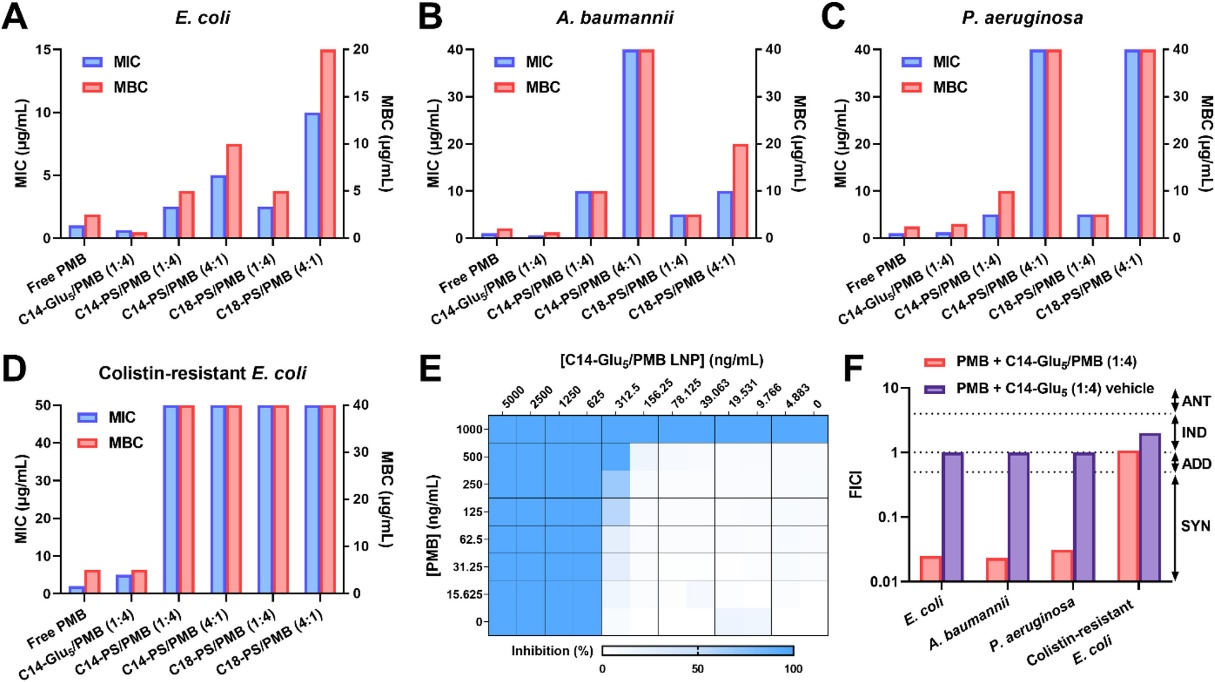
我们通过测定优化的PMB-LNP制剂对4种不同革兰氏阴性菌(大肠杆菌、鲍曼不动杆菌、铜绿假单胞菌和耐粘菌素大肠杆菌)的最低抑菌浓度(MIC)和最低杀菌浓度(MBC)来考察它们的抗菌性能。 在PMB-LNP制剂中,C14-Glu5/PMB (1:4) LNPs对所有测试细菌均表现出最强的抗菌活性,其MIC和MBC值最低(图2A-D)。 有趣的是,在电荷比为1:4时形成的PMB-LNPs,如C14-PS/PMB (1:4) 和C18-PS/PMB (1:4),在根除大肠杆菌、鲍曼不动杆菌和铜绿假单胞菌方面,比较电荷比为4:1时形成的PMB-LNPs更有效。 值得注意的是,在测试的制剂中,只有游离PMB和C14-Glu5/PMB (1:4) LNPs能有效抑制耐粘菌素大肠杆菌的生长(图2D)。 为研究游离PMB与C14-Glu5/PMB (1:4) LNPs之间的潜在协同作用,我们对所有革兰氏阴性菌进行了微量稀释棋盘法测定(图2E和S10)。 随后计算了协同抑制浓度指数(FICI)以确定协同作用的水平(表S4)。游离PMB和C14-Glu5/PMB (1:4) LNPs的组合对大肠杆菌、鲍曼不动杆菌和铜绿假单胞菌具有协同杀菌作用。 相比之下,游离PMB和C14-Glu5 (1:4) 载体组合则检测为无关作用(图2F)。 不出所料,耐粘菌素大肠杆菌对PMB治疗的敏感性较低,FICI值急剧增加证明了这一点。 这些结果表明,从C14-Glu5/PMB (1:4) LNPs释放的游离PMB分子与C14-Glu5/PMB (1:4) LNPs之间的协同效应可能至少部分促成了它们更优的抗菌效力。
3.3. 探索PMB-LNPs的杀菌机制
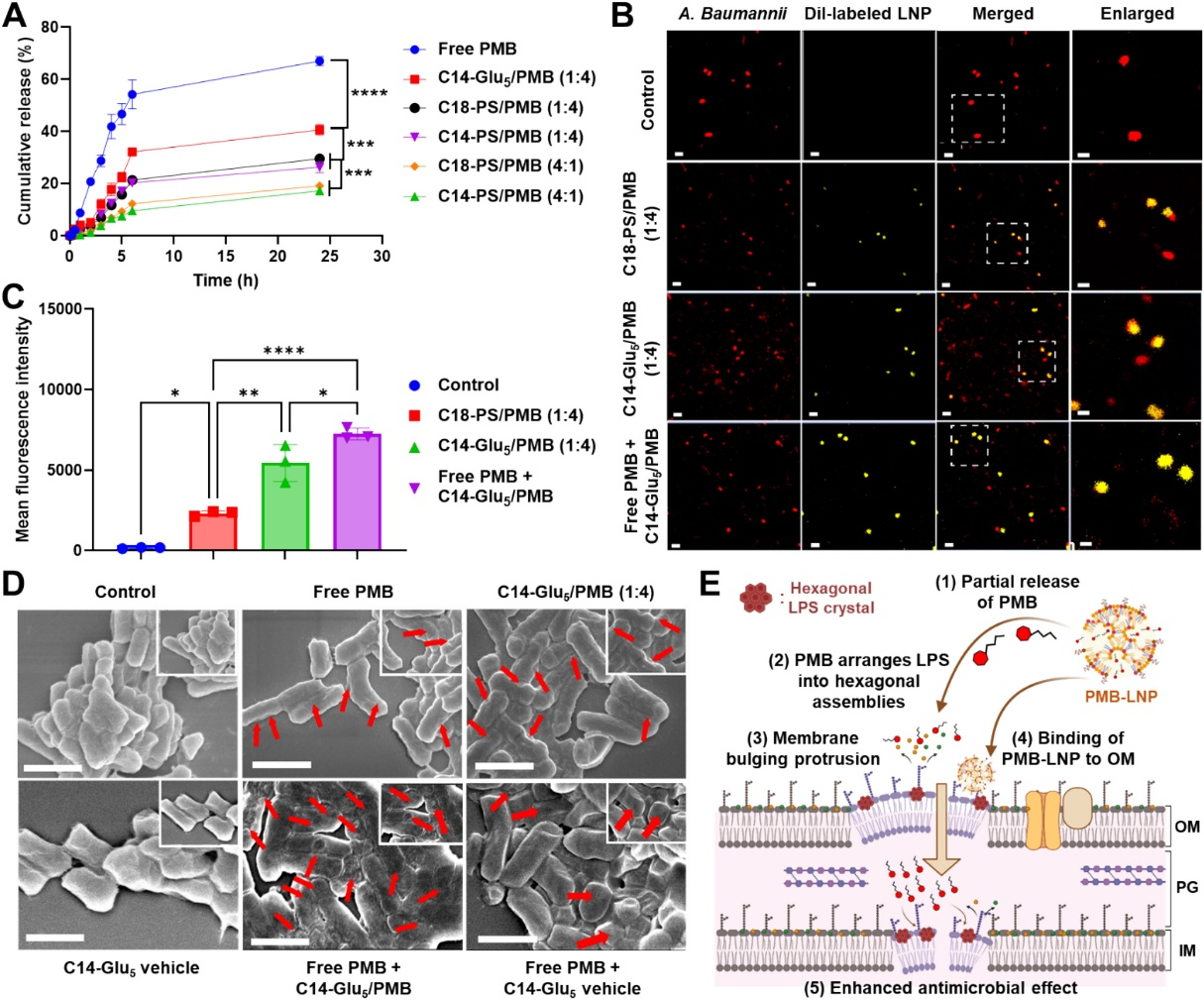
为了解C14-Glu5/PMB (1:4) LNP增强抗菌效果的机制,我们评估了优化的PMB-LNPs在 37℃下PBS (pH 7.4) 中的PMB释放动力学。 游离PMB迅速从透析盒中扩散出来,24小时后累积释放达到约67%(图3A)。 C14-Glu5/PMB (1:4) LNPs表现出显著 $(p<0.0001)$ 更慢的药物释放,这可能是由于包裹的PMB分子从LNP内部扩散延迟所致。 有趣的是,PMB的释放高度依赖于所掺入的阴离子脂质及其电荷比。 例如,在电荷比为4:1时形成的PMB-LNPs,如C14-PS/PMB (4:1) 和C18-PS/PMB (4:1),显示出比电荷比为1:4时形成的PMB-LNPs更持续的PMB释放。 电荷比为4:1时PBM释放较慢的原因,可能是阳离子PMB与大量存在的阴离子脂质之间更强的静电相互作用所致。
接下来,我们进行共聚焦激光扫描显微镜成像,以观察PMB-LNPs在细菌表面的结合情况。 选择鲍曼不动杆菌作为代表性革兰氏阴性菌,用0.2 mol% Dil标记的PMB-LNPs处理2小时。 细菌膜用红色荧光染料CellBrite Fix 640膜染料染色。。如图3B所示,用Dil标记的C14-Glu5/PMB (1:4) 或C18-PS/PMB (1:4) LNPs处理2小时后,鲍曼不动杆菌细胞表面可见黄色荧光,反映了它们与外膜的结合。在游离PMB与Dil标记的C14-Glu5/PMB (1:4) LNPs共同处理后,细菌表面的黄色荧光显著增强,证实了C14-Glu5/PMB (1:4) LNPs与游离PMB联合使用时,能更有效地在鲍曼不动杆菌的外膜上蓄积。 共同处理组中观察到的Dil荧光显著高于其他组(图3C),进一步证实了这一发现。 另一个有趣的发现是,C14-Glu5/PMB (1:4) LNPs具有比C18-PS/PMB (1:4) LNPs更强的膜结合能力。 考虑到C14-Glu5/PMB (1:4) LNPs的释放速度比C18-PS/PMB (1:4) LNPs快约3倍(图3A),C14-Glu5/PMB (1:4) LNPs增强的细菌结合能力可能归因于更大量的释放PMB导致外膜的改变增加。 这一特性也解释了C14-Glu5/PMB (1:4) LNPs更优的杀菌效果(图2B),因为表面结合的LNPs将允许PMB直接跨越外膜屏障进行局部递送,从而确保细菌暴露于更高的局部PMB浓度并产生治疗效果。
采用场发射扫描电镜(FE-SEM)直接观察鲍曼不动杆菌OM在暴露于PMB-LNPs后的形态变化。 如图3D所示,游离PMB处理在鲍曼不动杆菌表面诱导了隆起状突出,这与文献报道的PMB诱导的革兰氏阴性菌外膜生物物理变化一致 [51,52, 645]。游离PMB与C14-Glu5/PMB (1:4) LNPs共同处理引起了显著的膜扰动,表现为从细菌表面广泛突出的隆起。 然而,在游离PMB与C14-Glu5 (1:4) 载体共同处理时未观察到这种形态变化,这突显了游离PMB与C14-Glu5/PMB (1:4) LNPs协同作用对细菌膜破裂的重要性。
基于以上观察,C14-Glu5/PMB (1:4) LNPs一个可能的杀菌机制涉及一系列事件的发生:(i)PMB的部分释放及其与外膜上LPS的静电相互作用 [5],(ii)形成六边形LPS晶体使外膜变硬 [51,52],(iii)膜隆起突出,(iv)PMB-LNPs与受扰动外膜的结合增加 [30],以及(v)通过持续的局部PMB递送增强破坏效果(图3E)。 我们的共聚焦显微镜和SEM分析为所提出机制的初始步骤提供了实验支持,包括增强的细菌膜结合、纳米颗粒内化、部分PMB释放和早期膜破裂。 随后的阶段,以渐进性膜扰动和最终细菌细胞死亡为特征,是基于间接证据推断的,并得到了先前研究 [53,54] 的机理见解的支持。
3.4. PMB-LNPs改进的体外和体内生物相容性
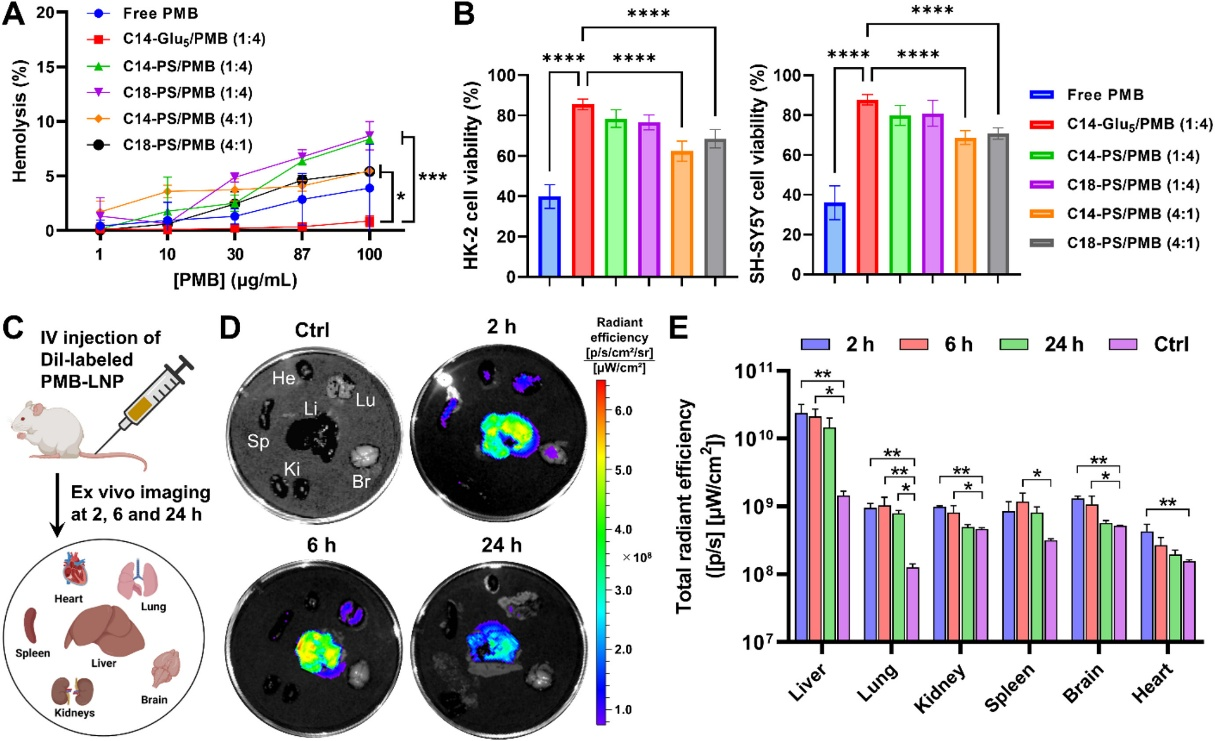
考虑到PMB-LNPs用于治疗血流细菌感染的潜在用途,我们使用新鲜采集的小鼠红细胞(RBCs)评估了它们的血液相容性。 不含PMB的空载体即使在 100ug/mL 的较高浓度下也未引起任何明显的溶血,证实了所有脂质组分对RBCs均无害。 另一方面,发现游离PMB以剂量依赖性方式引起溶血(图4A)。 在所有PMB-LNPs中,只有C14-Glu5/PMB (1:4) LNPs表现出可忽略的溶血活性,显著低于C14-PS/PMB (1:4) 和C18-PS/PMB (1:4) LNPs。
先前报道的临床研究表明,高剂量PMB单一疗法可通过PMB在肾脏和大脑中的主要蓄积以及随后在这些器官中断言细胞毒性作用而引起急性肾毒性和神经毒性 [7-10, 662]。 从这个角度出发,我们评估了PMB-LNPs对人近端肾小管上皮细胞系HK-2和人神经母细胞瘤细胞系SH-SY5Y的细胞相容性。游离PMB具有高毒性,在处理24小时内导致约60%的HK-2和SH-SY5Y细胞死亡(图4B)。 相反,用等剂量 300ug/mL的C14-Glu5/PMB (1:4) LNPs处理的细胞,观察到超过85%的细胞活力,表明其具有优越的细胞相容性。 有趣的是,在电荷比为1:4时形成的PMB-LNPs,如C14-PS/PMB (1:4) 和C18-PS/PMB (1:4),其细胞毒性低于电荷比为4:1时形成的PMB-LNPs。
我们进一步考察了Dil标记的C14-Glu5/PMB (1:4) LNPs在ICR小鼠静脉(IV)注射后的生物分布和药代动力学(图4C)。 注射后2小时、6小时和24小时,收集器官和血液进行离体荧光成像分析。 Dil荧光信号主要在2小时时在肝脏中观察到,而在肺、脾、脑和心脏中观察到较弱的信号(图4D)。 由于已知游离PMB主要在肾脏和大脑中蓄积 [9,10],因此将PMB包裹到LNPs中可能将其生物分布转向了肝脏。 观察到的PMB-LNPs在肝脏中的优先蓄积与全身给药LNPs的已知生物分布模式一致。 这种肝脏靶向性主要归因于载脂蛋白E(ApoE)在LNP表面的吸附,促进了肝细胞通过低密度脂蛋白(LDL)受体的摄取 [57,58, 755]。
我们的药代动力学研究显示,C14-Glu5/PMB (1:4) LNPs的循环半衰期为7.3小时,远长于文献报道的游离PMB(1小时) [24, 756]。 C14-Glu5/PMB (1:4) LNPs的血液循环时间延长可能归因于其PEG化的表面,这可以减少肾小球滤过过程和被单核吞噬细胞系统的识别 [40]。 注射后2小时,所有器官的荧光信号随时间逐渐减弱,反映了C14-Glu5/PMB (1:4) LNPs从体内的清除。 收集器官中总辐射效率的定量分析进一步支持了这一观察结果(图4E)。 到IV注射后24小时,肾脏、脾脏、心脏和大脑的总辐射效率值降低到与模拟对照组相当的水平,这意味着C14-Glu5/PMB (1:4) LNPs几乎完全从这些器官中清除。 除了相对较低的肾脏和大脑蓄积外,C14-Glu5/PMB (1:4) LNPs的完全清除将有利于降低诱导致命性肾毒性和神经毒性的风险。 研究发现PMB-LNPs的最低致死剂量 >11.85~mg/kg高于小鼠中游离PMB的最低致死剂量 5.61~mg/kg,这表明当PMB被包裹在LNPs内部时,其脱靶毒性大大减轻了(表S7)。 总之,这些结果证明了C14-Glu5/PMB (1:4) LNPs比游离PMB具有更优的细胞相容性和体内耐受性。
3.5. 在中性粒细胞减少性小鼠菌血症模型中的治疗功效
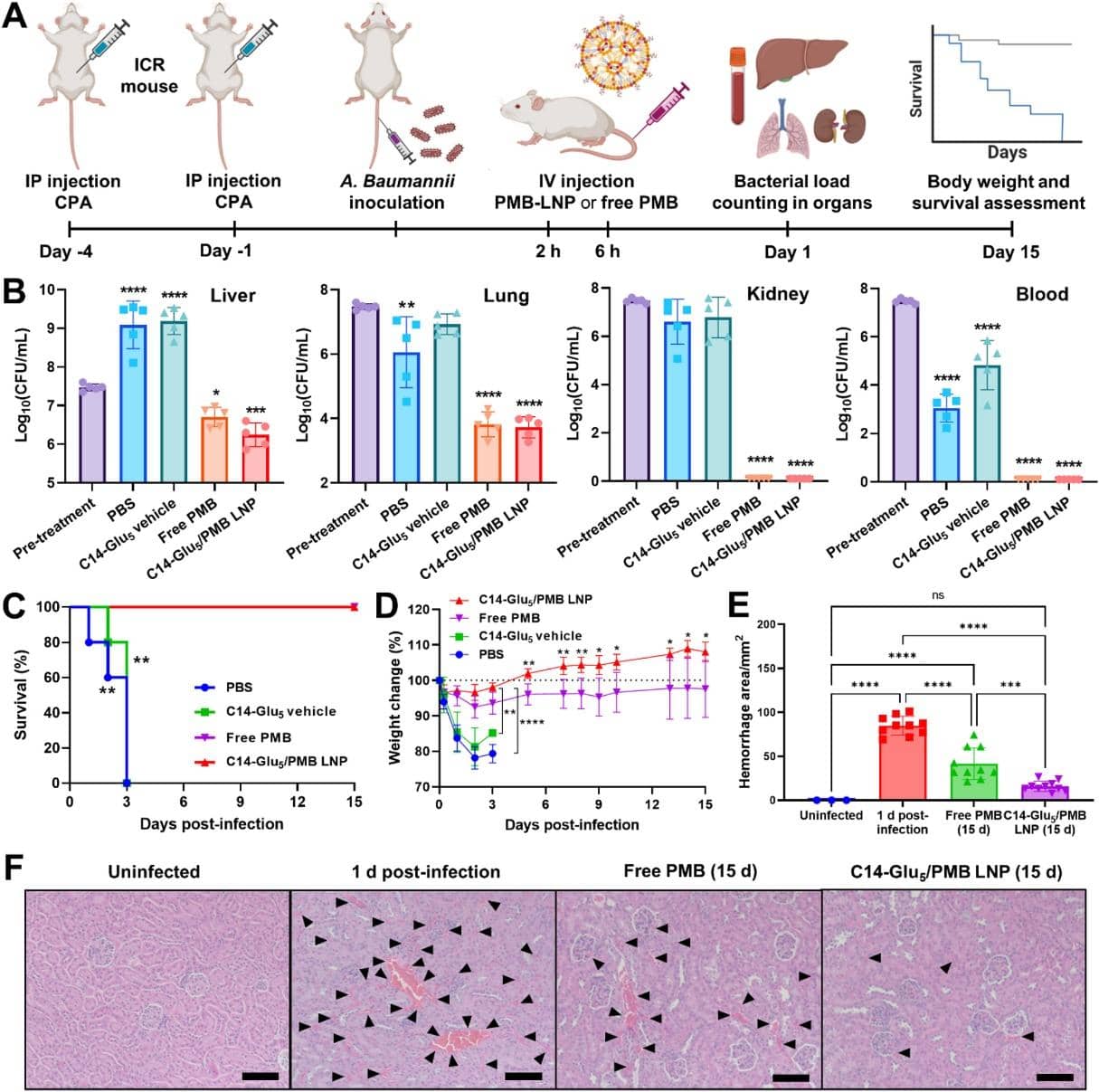
在小鼠中性粒细胞减少的鲍曼不动杆菌菌血症模型中考察了C14-Glu5/PMB LNPs的体内有效性。 在细菌接种前1天和4天,通过腹腔(IP)注射免疫抑制剂环磷酰胺(CPA),使雌性ICR小鼠发生中性粒细胞减少(图5A)。 通过IV接种106 CFU/小鼠剂量的鲍曼不动杆菌建立血流感染,因为该细菌剂量能使中性粒细胞减少的ICR小鼠存活至少24小时。 接种后2和6小时,小鼠被随机分配接受IV注射游离PMB 5mg/kg 或C14-Glu5/PMB LNP 5mg/kg、等效剂量的C14-Glu5载体或PBS作为对照。
感染后第1天,在肝脏、肺、肾脏和血液中检测到大量鲍曼不动杆菌,表明其广泛定植(图5B)。 与C14-Glu5载体和PBS组相比,游离PMB和C14-Glu5/PMB LNP均使小鼠体内的细菌负荷显著降低。 例如,在肺、肾脏和血液中,细菌计数减少了超过3个对数(>99.9%的细菌被消除)。 在肝脏中,经过2剂C14-Glu5/PMB LNP的单次治疗方案后,第1天有超过90%的细菌被根除。 值得注意的是,C14-Glu5/PMB LNP在肝脏中的细菌计数比较游离PMB低约2.9倍。 C14-Glu5/PMB LNPs在肝脏中的主要蓄积(图4D和E)被认为是其比较游离PMB更有效地根除肝脏驻留细菌的原因。
用C14-Glu5载体治疗的感染小鼠在3天内迅速死亡,而用游离PMB或C14-Glu5/PMB LNP治疗的小鼠存活了至少15天(图5C)。 尽管存活率相当高,但 C14-Glu5/PMB LNP组的体重变化与游离PMB组相比表现出显著差异(图5D)。 接种鲍曼不动杆菌后2天,观察到体重减轻>20%,反映了其有害的副作用。 不出所料,C14-Glu5载体治疗并未显著减缓体重减轻。 用C14-Glu5/PMB LNPs治疗的小鼠在4天内体重恢复。 相比之下,游离PMB治疗组的小鼠直到15天终点仍未能恢复初始体重,这表明接受游离PMB治疗的小鼠并未完全从鲍曼不动杆菌引起的损伤中恢复。
为进一步检查细菌引起的损伤,分别收集了器官和血液进行组织学和临床化学分析。 通过苏木精-伊红(H&E)染色,我们观察到鲍曼不动杆菌感染后第1天,肾脏的肾小管间有广泛出血(图5E和F)。 值得注意的是,图5F中黑色箭头突出的区域表明肾脏组织内有明显的细菌浸润和相关的炎症反应。 这些标记区域代表了由细菌感染引起的局灶性组织损伤区域,其特征是大量的炎症细胞募集、肾小管变性和局部坏死性变化。 我们的观察结果与先前报道患有鲍曼不动杆菌感染的人类患者出血增加的研究非常一致 [59,60, 898]。
重要的是,在15天终点时,用C14-Glu5/PMB LNPs治疗的小鼠的肾小管间出血程度显著 $(p<0.001)$ 低于用游离PMB治疗的小鼠。 考虑到游离PMB和C14-Glu5/PMB LNP均在很大程度上将肾脏中的细菌负荷减少到几乎检测不到的水平(图5B),肾脏出血很可能是由在抗生素治疗中存活下来的残留细菌再生长引起的。 因此,我们可以从我们的观察中推断,C14-Glu5/PMB LNP在抑制鲍曼不动杆菌在肾脏中再生长方面,其效果比游离PMB更持久。 基于药代动力学数据(图S14),C14-Glu5/PMB LNPs的延长功效可能源于其延长的全身循环。 用游离PMB或C14-Glu5/PMB LNPs治疗后,血清肌酐水平(一个众所周知的肾功能标志物 [61])显著降低,进一步证实了这一发现(图S15A)。 在15天终点时,游离PMB和C14-Glu5/PMB LNPs治疗组的血清肌酐水平与未感染组相似 $(p>0.05)$。 此外,发现C14-Glu5/PMB LNP和游离PMB治疗能将血清丙氨酸转氨酶(ALT,一种肝功能标志物)水平恢复到正常水平(图S15B)。 与临床化学结果一致,肝脏和肺的组织学分析显示,在终点时没有与细菌感染相关的组织异常(图S16)。
综上所述,以上结果表明,C14-Glu5/PMB LNPs能有效减少血液和器官中的细菌负荷,并提高了感染鲍曼不动杆菌的中性粒细胞减少小鼠的存活率,且在评估的时间点内未出现任何显著的体重减轻和器官损伤。 尽管这些结果支持了PMB-LNPs的治疗潜力,但我们承认存在与肝脏蓄积相关的风险,包括肝毒性和脱靶效应,特别是在重复或长期暴露的情况下。 因此,全面的长期毒性评估对于充分表征PMB-LNPs的安全性特征并支持其向临床应用推进至关重要。
五. 研究结论
本文成功制备并筛选了一系列包裹PMB的脂质纳米颗粒(PMB-LNPs),以期更有效、更安全地治疗革兰氏阴性菌感染。 阴离子脂质中带负电荷的基团与PMB中带正电荷的基团之比对PMB-LNPs的Z-平均粒径、zeta电位、释放动力学和抗菌活性有显著影响。 经过体外筛选评估,我们确定C14-Glu5/PMB (1:4) LNP为主要制剂,因为它在所有PMB-LNPs中对一组革兰氏阴性菌表现出最强的广谱杀菌性能。 机制研究表明,C14-Glu5/PMB (1:4) LNPs中PMB的部分释放可能有助于其对大肠杆菌和鲍曼不动杆菌产生优于游离PMB的抗菌效力。 更重要的是,将PMB包裹在LNPs中改善了其细胞相容性、体内耐受性和药代动力学。 在鼠类中性粒细胞减少的鲍曼不动杆菌菌血症模型中,通过静脉注射C14-Glu5/PMB (1:4) LNPs治疗,有效减少了主要器官中的细菌负荷。 它们延长了存活期,且未出现任何显著的体重减轻。 此外,通过组织学和临床化学分析检查,C14-Glu5/PMB LNP在抑制鲍曼不动杆菌在肾脏中再生长方面比游离PMB更有效。 这些发现可为设计基于LNP的抗菌纳米药物提供宝贵的见解,以有效治疗由革兰氏阴性菌引起的传染病。
六、创新与局限性
(一)创新点
研究团队引入了一种新颖的LNP制剂策略,利用阴离子脂质通过静电相互作用 ,来包裹和递送阳离子大分子抗生素;设计并合成了一种新型的阴离子脂质C14-Glu5;C14-Glu5/PMB (1:4) LNP能够有效抑制耐粘菌素的大肠杆菌。
(二)局限性
研究团队提出了一个协同杀菌机制,该机制的后续阶段(如渐进性的膜破裂和最终的细菌死亡)是基于间接证据推断的;
LNP制剂主要蓄积在肝脏可能会带来肝毒性或脱靶效应的风险;
由于高浓度LNP制剂的溶解度有限,研究未能测试高于 11.85 mg/kg 的PMB-LNP剂量 。
七、学术与应用启发
突破了LNP(脂质纳米颗粒)主要用于递送核酸(带负电)的传统模式;在设计纳米系统时,可以利用药物与载体之间的协同效应,实现“1+1>2”的治疗效果。
文献原文:


