内皮细胞STING和STAT1介导内毒素血症诱导休克模型中IL-6的干扰素非依赖性作用
作者:Nina Martino, Erin K. Sanders, Ramon Bossardi Ramos等
doi:https://doi.org/10.1172/JCI189570

文章概述
本文聚焦内毒素血症休克模型中IL - 6信号下游通路。通过对小鼠和人内皮细胞实验,发现内皮细胞中IL - 6通路抑制剂SOCS3缺失会促进I型干扰素样基因特征表达。IL - 6以非经典、不依赖干扰素方式诱导基因表达,需STAT1、cGAS、STING和IRFs等参与。抑制该通路可减轻内毒素血症严重程度,为控制IL - 6细胞内反应、调节炎症反应提供新思路。
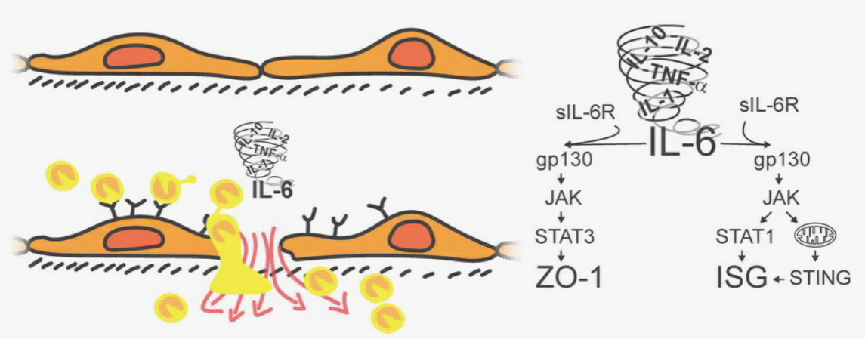
研究背景
严重全身性炎症反应常引发多器官功能障碍,细胞因子“风暴”导致血管功能障碍。IL - 6循环水平与疾病严重程度和休克死亡率相关,但其促进内皮功能障碍和器官损伤机制不明。此前研究发现IL - 6信号使内皮通透性增加,SOCS3可抑制此过程,但SOCS3易被降解。且内皮特异性SOCS3敲除小鼠LPS攻击后有严重血管病变、肾衰竭及I型干扰素样反应,而IL - 6诱导该反应机制未知,因此开展本研究。
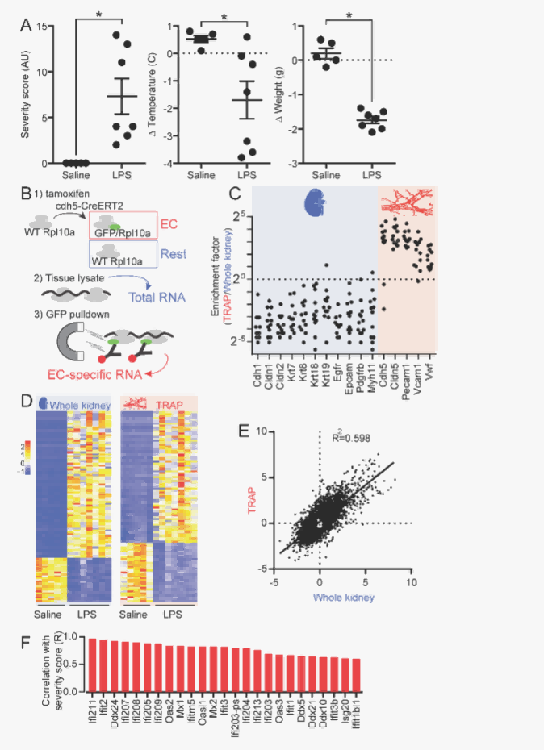
研究结果
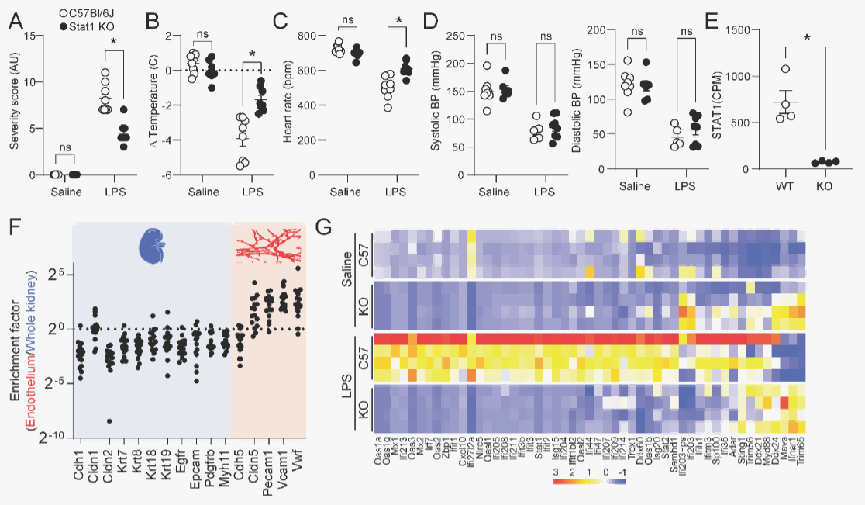
急性内毒素血症使肾内皮细胞强烈表达ISG,内皮SOCS3缺失增强ISG表达。 LPS能够诱导小鼠产生炎症反应,引起严重程度增加、体温降低和体重减轻等生理变化。揭示了肾脏组织中不同基因在TRAP和全肾中的富集差异,以及LPS处理对全肾和TRAP中基因表达的影响。发现全肾和TRAP中的基因表达存在一定相关性,同时筛选出了与炎症严重程度相关的基因,为后续研究炎症机制提供了基因层面的线索。
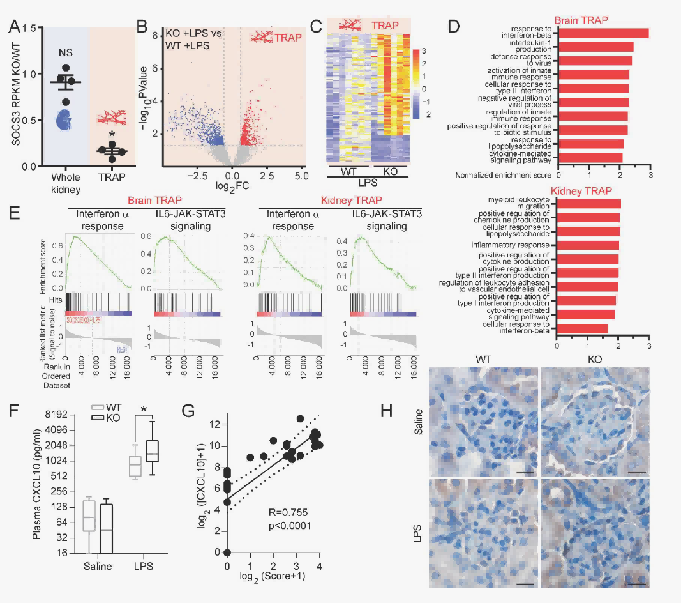
该图表整体呈现了SOCS3基因敲除(KO)小鼠在脂多糖(LPS)刺激下,与野生型(WT)小鼠相比,在肾和脑的特定组分(TRAP)中基因表达、免疫反应和信号通路的变化情况,以及血浆中细胞因子(如CXCL10)的浓度变化和肾组织的病理变化,突出了SOCS3在调节免疫反应和相关信号通路中的重要作用
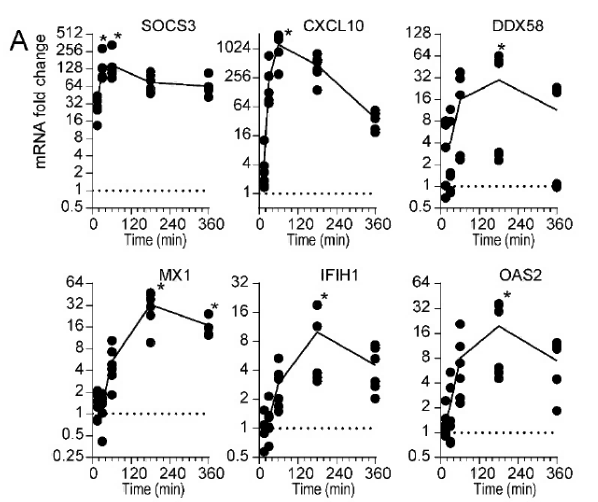
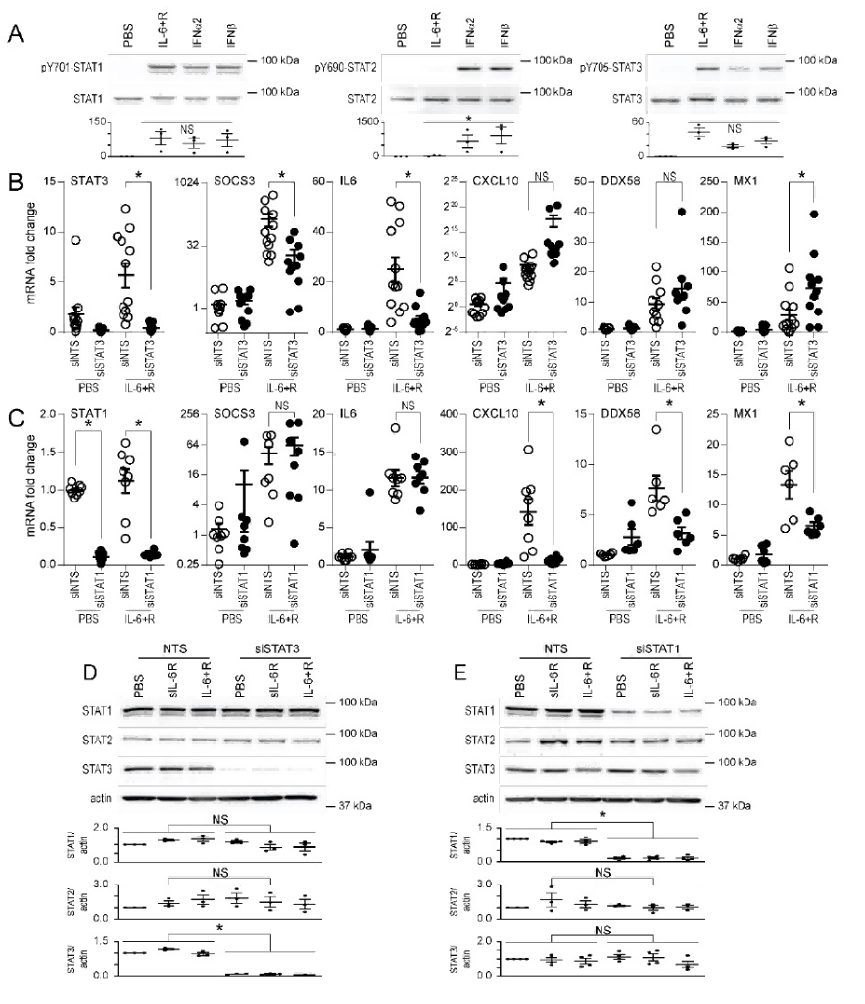
IL - 6诱导人脐静脉内皮细胞(HUVEC)表达ISG不依赖IFNAR1表达。
图表A展示了在特定实验条件下,多个基因(SOCS3、CXCL10等)的mRNA表达水平随时间的动态变化,表明这些基因在不同时间点的表达调控情况。图表B检测了不同处理组(PBS、IL - 6 + R、IFNβ)下相关蛋白(IFNβ、IRF1等)的表达情况,该图表反映了IL - 6 + R和IFNβ处理对相关基因转录和蛋白表达的调控作用。
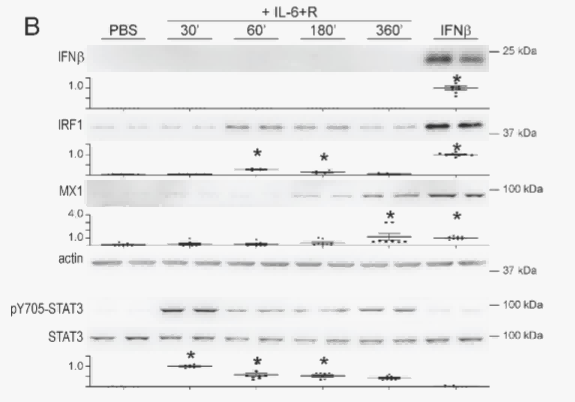
IL - 6诱导HUVEC表达ISG需STAT1,但不依赖STAT3。
图表A展示了在特定实验条件下,多个基因(SOCS3、CXCL10等)的mRNA表达水平随时间的动态变化,表明这些基因在不同时间点的表达调控情况。图表B检测了不同处理组(PBS、IL - 6 + R、IFNβ)下相关蛋白(IFNβ、IRF1等)的表达情况,该图表反映了IL - 6 + R和IFNβ处理对相关基因转录和蛋白表达的调控作用。
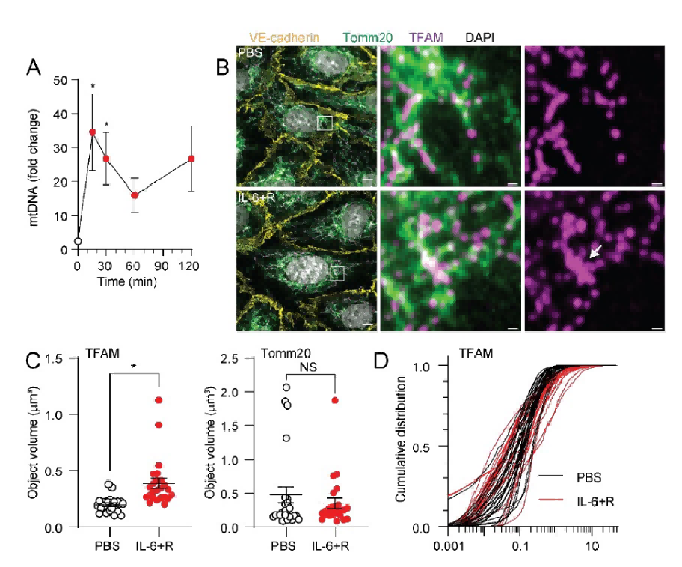
IL - 6诱导ISG表达涉及线粒体DNA释放及cGAS、STING激活。
IL - 6 + R处理可以影响细胞中线粒体相关指标、可引起mtDNA含量在不同时间点的动态变化、影响TFAM在线粒体上的分布和其对象体积,而对线粒体膜蛋白Tomm20的对象体积无显著影响。这些结果可能暗示IL - 6 + R处理通过影响TFAM与线粒体的关联,进而影响线粒体的功能或状态。
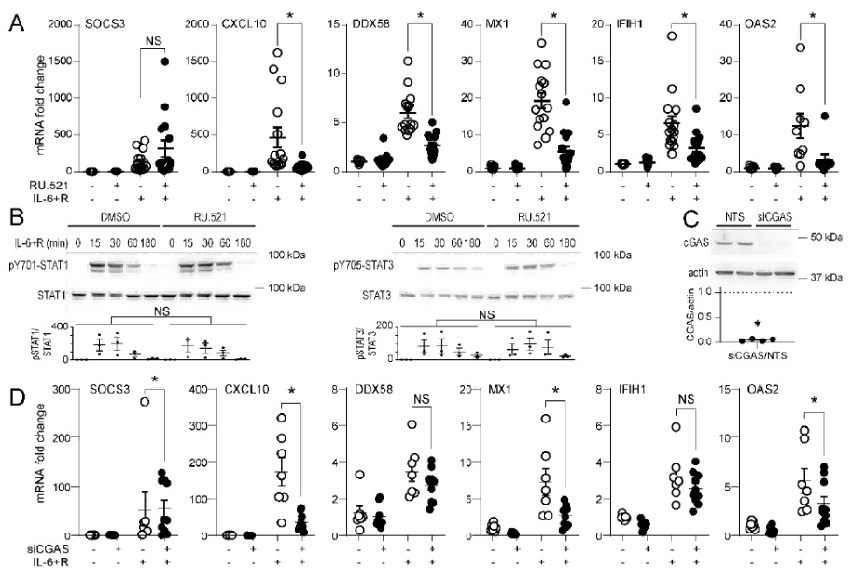
RU.521对IL - 6 + R诱导的部分基因(如CXCL10等)的mRNA表达有显著影响,可能起到增强作用,但对STAT1和STAT3的磷酸化水平影响不显著。siCGAS处理显著降低了cGAS蛋白的表达水平,并且对IL - 6 + R诱导的部分基因(如SOCS3等)的mRNA表达也有显著影响,表明cGAS可能参与了IL - 6 + R相关的基因表达调控过程。 这些结果为进一步研究细胞信号通路和基因表达调控机制提供了数据支持。
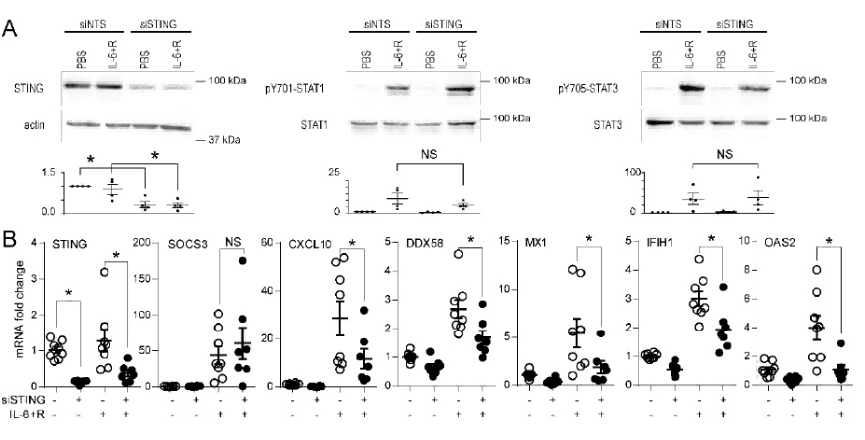
敲低STING(siSTING处理)能够显著降低STING蛋白和相关基因(如CXCL10、DDX58、MX1、IFI1H1、OAS2等)的mRNA表达水平,而对STAT1和STAT3的磷酸化水平没有显著影响。这暗示STING在调控这些基因表达中发挥重要作用,可能参与相关的免疫或炎症信号通路,但对STAT1和STAT3的磷酸化调控影响较小。
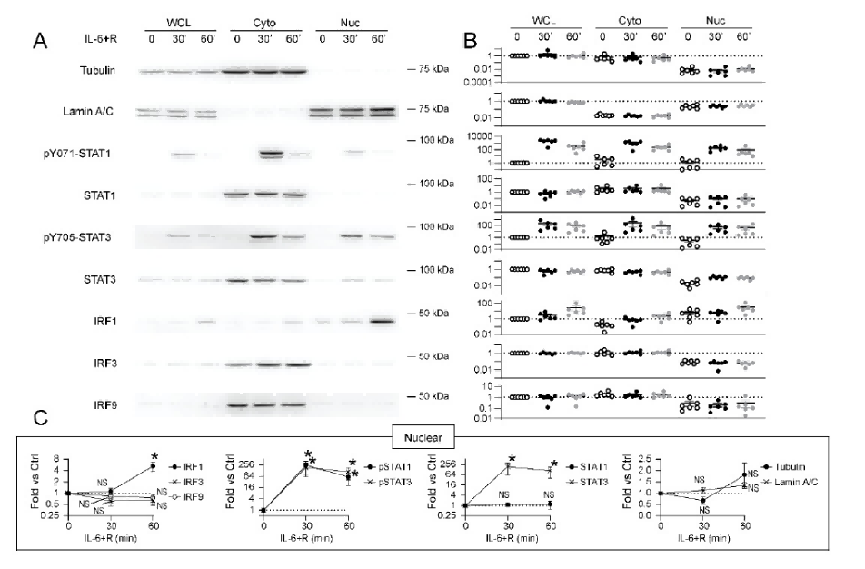
IRF1和IRF3介导IL - 6信号下游转录变化。
IL - 6刺激能够诱导STAT1的磷酸化和核转位,同时影响IRF1等干扰素调节因子在细胞核中的表达,暗示IL - 6信号通路与免疫和炎症反应相关基因的转录调控存在关联。而STAT3以及其他IRF(如IRF3、IRF9)在该实验条件下的变化不明显
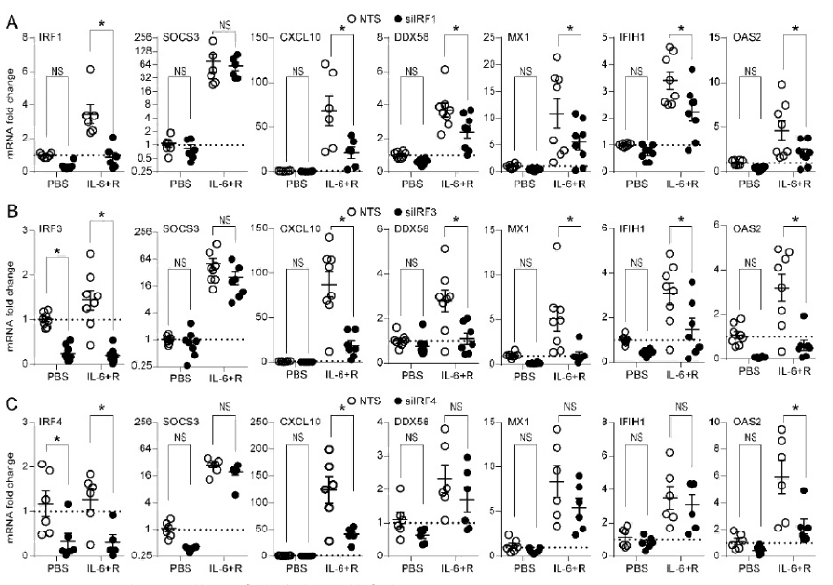
IL - 6+R处理能够影响多种基因(包括IRF1、IRF3、IRF4、CXCL10、DDX58、MX1、IFI1H、OAS2等)的mRNA表达水平,并且干扰IRF1、IRF3、IRF4基因后,这种影响可能会发生改变。而SOCS3基因的表达似乎不受IL - 6+R处理以及IRF基因干扰的显著影响
内皮STING或STAT1缺失减轻LPS攻击严重程度,降低内皮ISG表达。
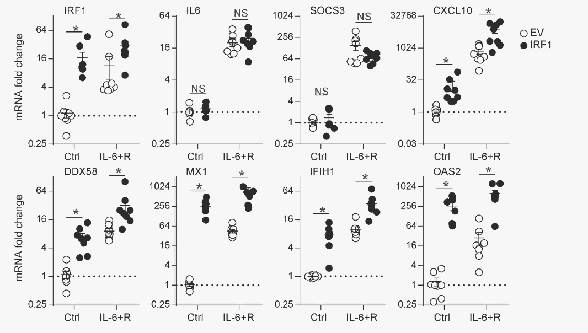
IRF1在IL - 6+R处理的情况下,能够特异性地促进一系列基因(包括自身)的mRNA表达上调,而对另外一些基因(如IL6和SOCS3)无明显调控作用。STING基因敲除显著降低了肾脏相关的严重程度评分和温度变化。LPS刺激下,两组之间存在差异。
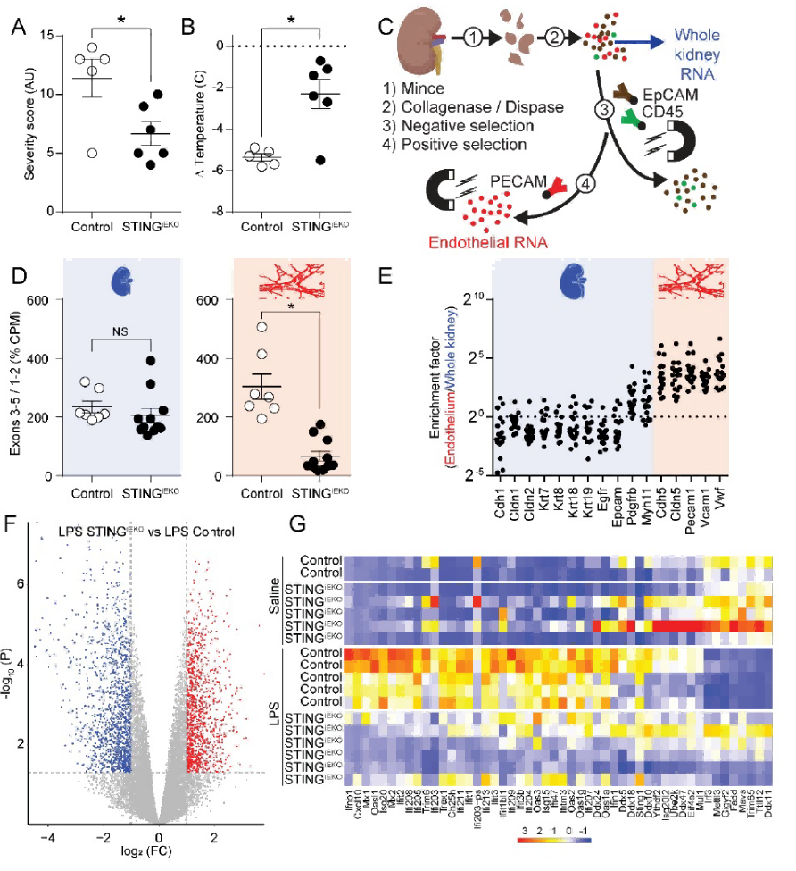
Stat1基因敲除小鼠在LPS处理后,表现出较低的严重程度评分、较小的体温下降和心率增加,表明Stat1在LPS诱导的炎症反应中起重要作用。Stat1 KO小鼠的STAT1蛋白表达显著降低,验证了基因敲除的有效性。基因富集和表达热图展示了不同基因在野生型和Stat1 KO小鼠中的表达差异。这些结果表明,敲除Stat1基因可以减轻炎症反应的严重程度。
研究结论、不足与展望
研究结论:本文发现内毒素休克时肾和脑内皮细胞存在受SOCS3限制的I型干扰素样特征表达,由Sting1和Stat1促进。IL - 6触发线粒体DNA释放,通过cGAS/STING非经典途径,依赖IRF1和IRF3促进ISG表达,且通透性和DNA感应反应由该细胞因子下游平行途径驱动。
研究的创新性:揭示IL - 6以非经典、不依赖干扰素方式诱导ISG表达,发现其信号下游新通路,为炎症反应机制提供新见解,为治疗炎症相关疾病提供潜在靶点。
研究的不足之处:研究采用内毒素血症模型,未完全模拟脓毒症;仅评估单次时间点的内皮反应;不能排除其他应激传感器作用;未明确IFN样转录反应与器官损伤因果关系。
研究展望:在已建立的脓毒症模型中验证结果;深入分析内皮反应动力学;研究其他应激传感器作用;明确IFN样转录反应与器官损伤因果关系,为治疗脓毒症休克提供更有效策略。
研究意义:有助于理解细胞因子信号下游调节内皮功能障碍机制,为开发靶向细胞因子信号下游、调节内皮功能障碍的治疗方法奠定基础,有望改善脓毒症患者预后。
文献原文:


