Redox Biology 西南医科大学周军教授团队揭示YAP/Nrf2抑制铁死亡减轻肠缺血再灌注引起的急性肺损伤
肠道缺血再灌注(Intestinal ischemia reperfusion,II/R)是临床实践中常见的危重疾病。II/R不仅会导致局部肠道损伤,还会破坏肠道屏障功能并促进肠道菌群移位,进而引发全身性炎症反应和远端器官功能障碍。在这些器官中,肺部对II/R尤为敏感,常导致急性肺损伤(acute lung injury,ALI)的发生。
2025年8月,西南医科大学周军教授团队在Redox Biology 杂志发表题为“YAP/Nrf2 suppresses ferroptosis to alleviate acute lung injury induced by intestinal ischemia/reperfusion”的研究型论文,揭示了YAP在II/R诱导的ALI中具有重要作用,可以通过与Nrf2结合并促进其核转位,从而减轻ALI后铁死亡。该研究提示YAP可作为减轻ALI的靶蛋白,具有重要的临床意义。
|
|
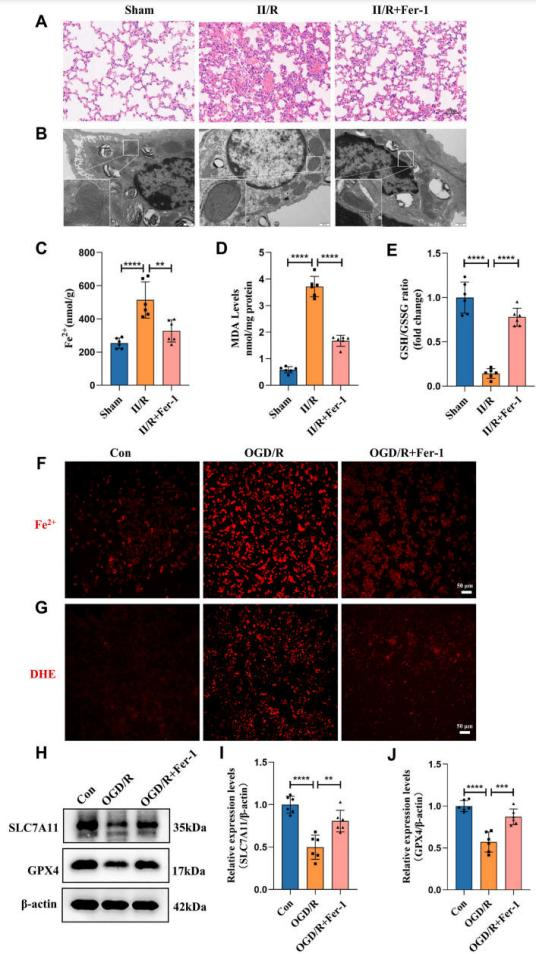
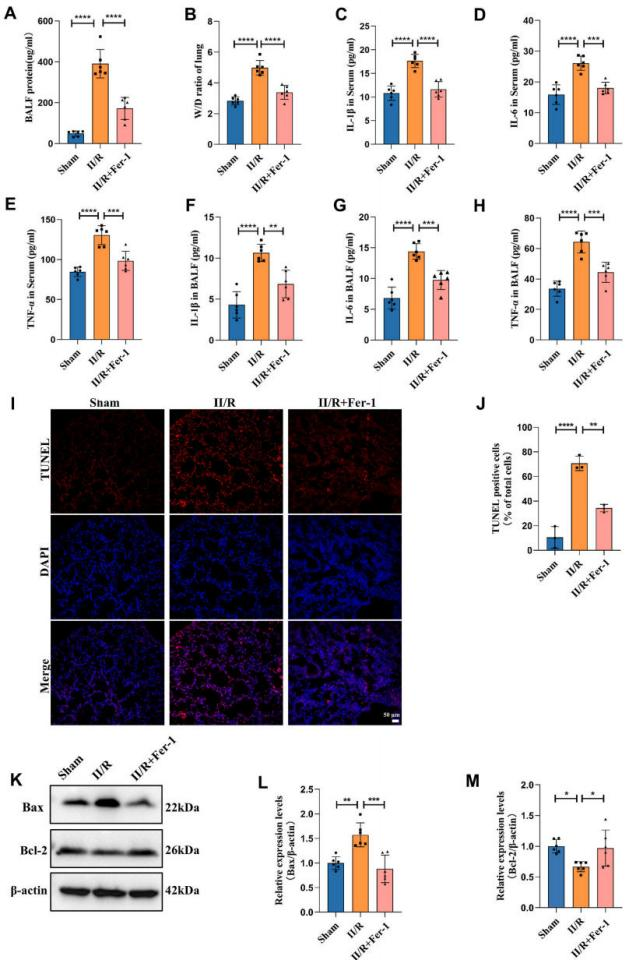
为了探究铁死亡在II/R诱导的ALI中的作用,研究团队给予铁死亡抑制剂铁抑素Fer-1进行II/R小鼠以及肺上皮细胞MLE-12氧糖剥夺再复氧(oxygen-glucose deprivation and reoxygenation, OGD/R)的干预。研究发现,Fer-1可以减轻II/R以及OGD/R诱导的ALI程度,减轻Fe2+和活性氧的蓄积,并减轻ALI后血清和肺泡灌洗液(bronchoalveolar lavage fluid,BALF)中的炎症因子水平和凋亡。
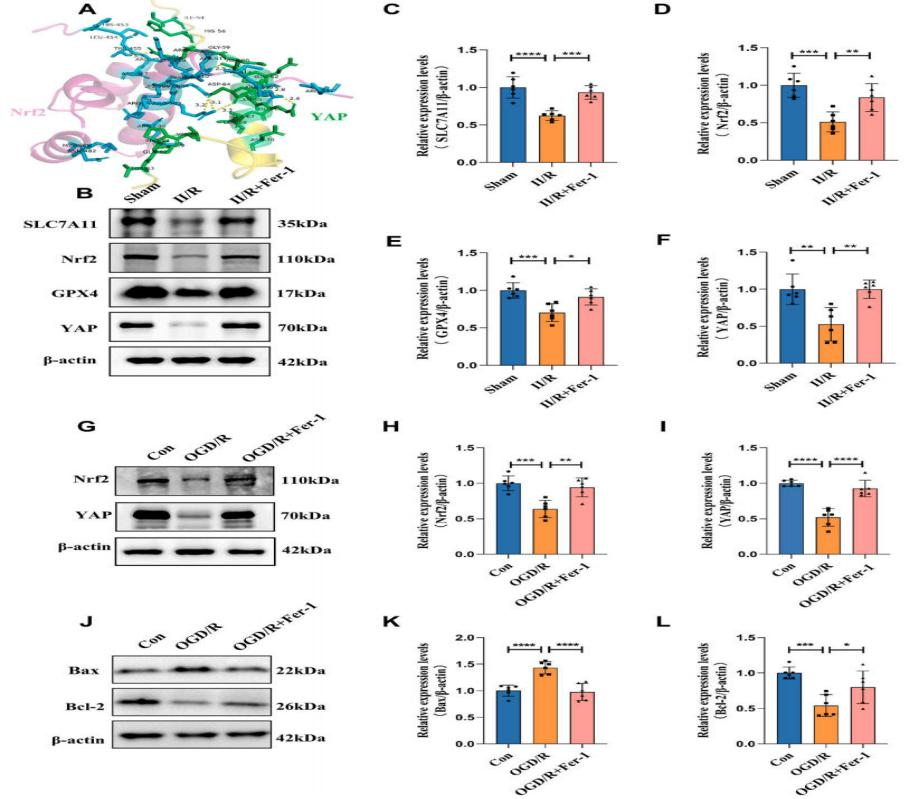
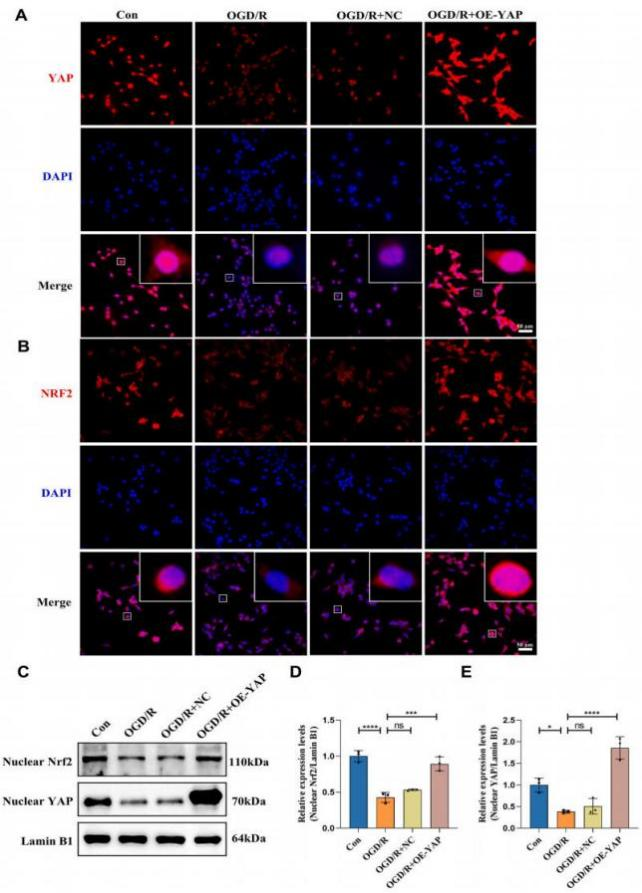
基于最新YAP同源蛋白TAZ的研究表明,在减轻炎症和增强小胶质细胞抗氧化能力方面,TAZ与Nrf2存在直接功能相互作用。因此,考虑YAP与Nrf2之间可能存在直接和间接的关联。为验证这一假设,研究人员首先对YAP和Nrf2进行了分子对接分析,发现这两种蛋白具有多个结合位点。并检测了YAP及铁死亡负调控蛋白(包括GPX4、Nrf2和SLC7A11)的表达水平。结果显示,在II/R模型中YAP、Nrf2、GPX4和SLC7A11的表达量显著降低,但经Fer-1干预后部分恢复。此外,细胞模型中Nrf2和YAP的表达水平与动物模型观察结果一致。这些结果表明,铁死亡参与了II/R诱导的II/R后ALI过程。
|
|
|
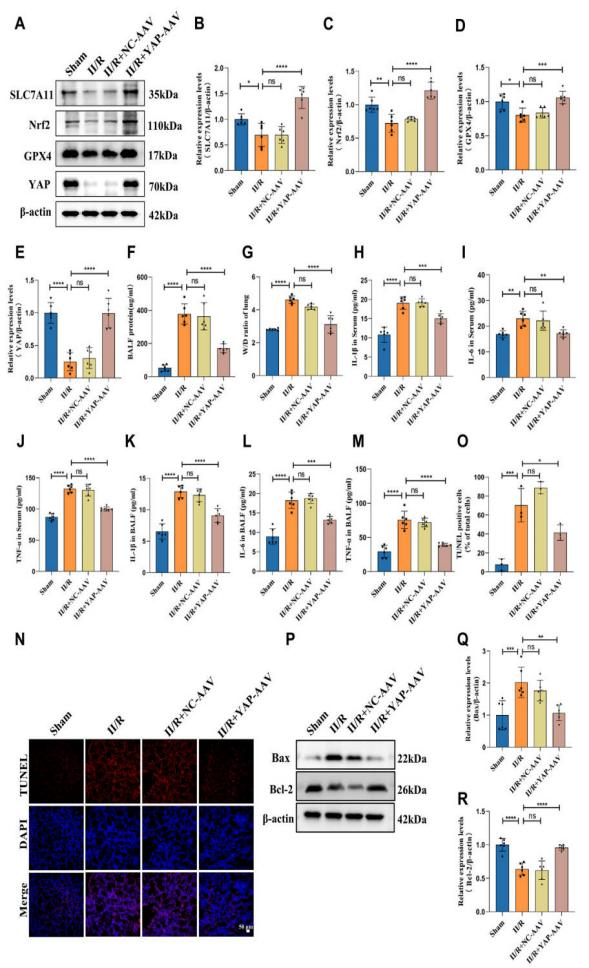
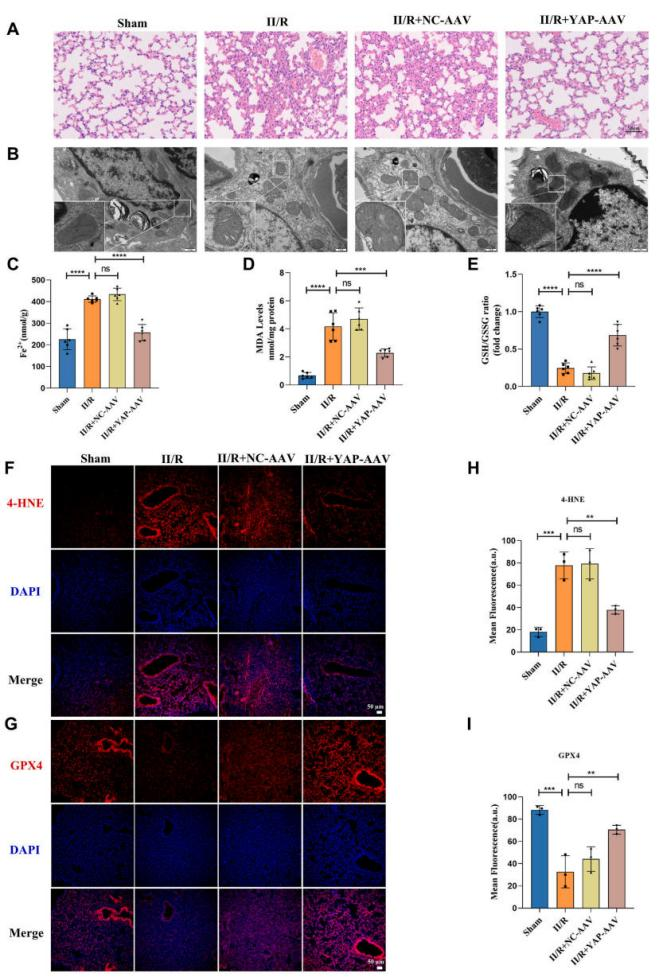
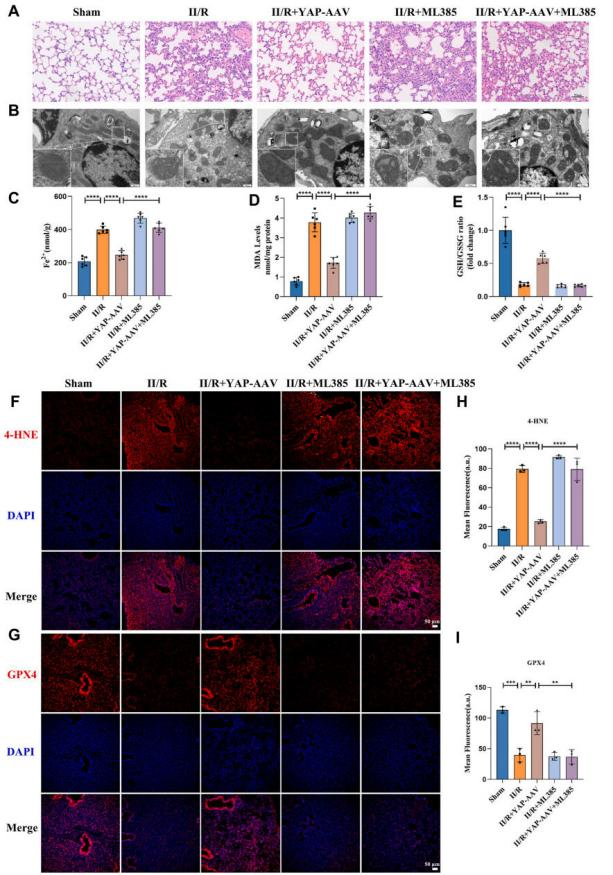
为深入阐明YAP在铁死亡及II/R诱导的ALI中的作用,本研究采用腺相关病毒(AAV)在小鼠体内过表达YAP。值得注意的是,YAP的过表达显著缓解了肺组织损伤,表现为肺出血减少和肺泡壁增厚等ALI特征性病理改变明显改善。透射电镜观察显示,YAP过表达逆转了II型肺泡上皮细胞因急性肺损伤引发的线粒体铁死亡典型改变。与II/R组相比,II/ R + YAP-AAV组的Fe2+和MDA水平显著降低,同时谷胱甘肽/还原型谷胱甘肽比值(GSH/GSSG)升高,GPX4水平下降和脂质过氧化的主要代谢产物4-羟基-2-壬烯醛(4-HNE)升高的现象。
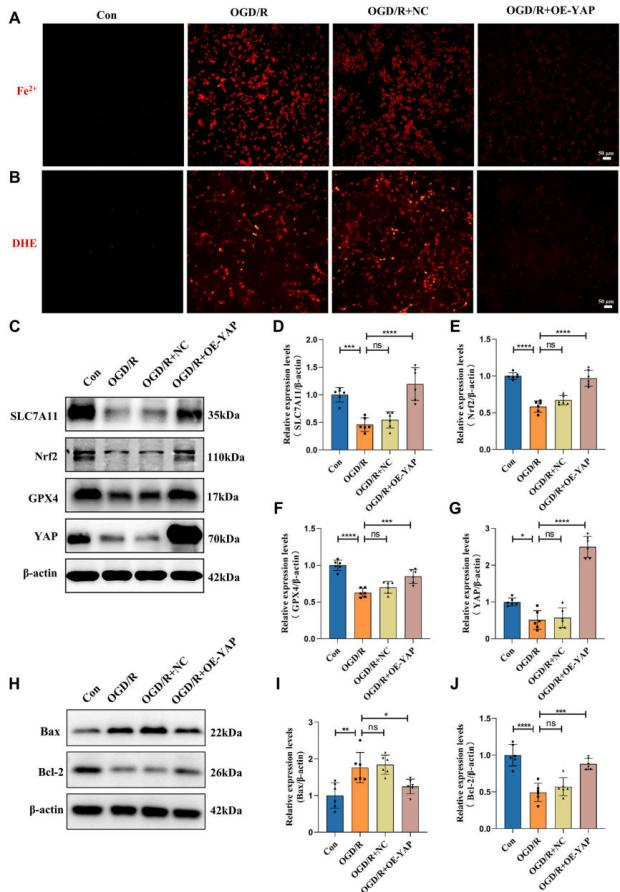
为分析YAP核蛋白特性,研究人员进行了核质分离实验,并通过蛋白质印迹和免疫荧光技术进一步研究其核定位。观察发现,YAP的过表达主要促进细胞核增殖,并推动Nrf2蛋白向细胞核转移。YAP抑制铁死亡并减轻肺损伤后炎症和凋亡。细胞模型中趋势与动物模型相一致。
|
|
|
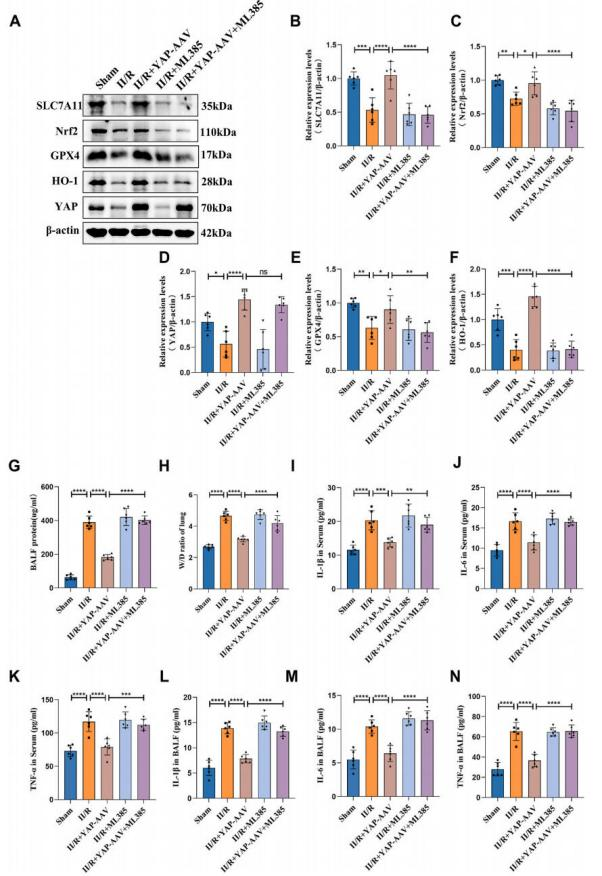
为验证YAP的保护作用源于Nrf2激活,研究团队使用Nrf2特异性抑制剂ML385对小鼠进行预处理。首先,HE染色结果显示:抑制Nrf2可逆转YAP对II/R诱导的ALI的保护作用。通过透射电镜观察肺部II型肺泡上皮细胞线粒体发现,当Nrf2被抑制时,YAP对铁死亡的保护作用被阻断。此外,免疫荧光检测Fe2+、GSH/GSSG、丙二醛(MDA)以及4-羟基壬烯酸(4-HNE)和GPX4的表达水平进一步支持上述结论,证实Nrf2抑制会削弱YAP的抗脂质氧化功能。其次,western blot检测显示ML385能有效抑制Nrf2、GPX4、SLC7A11及下游蛋白HO-1的表达,但YAP的过表达水平未受Nrf2抑制剂影响。最后,炎症因子分析结果表明,抑制Nrf2可逆转YAP的保护作用。
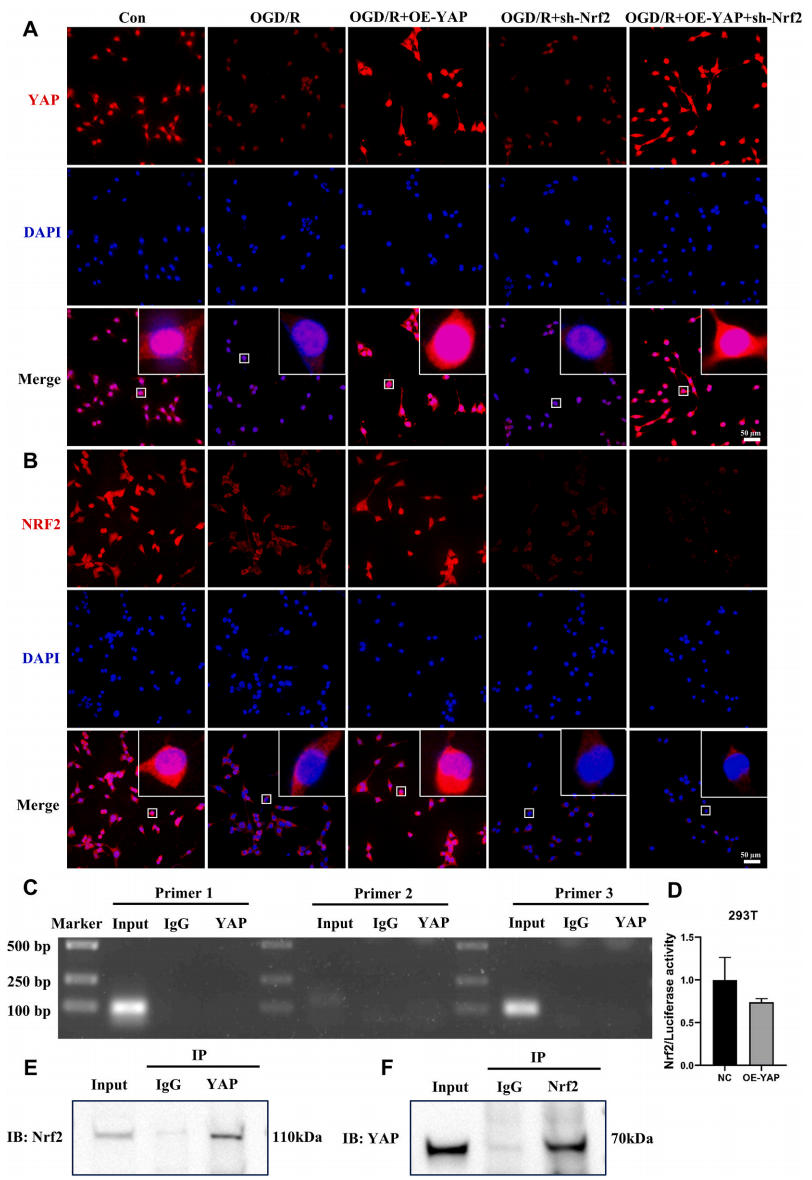
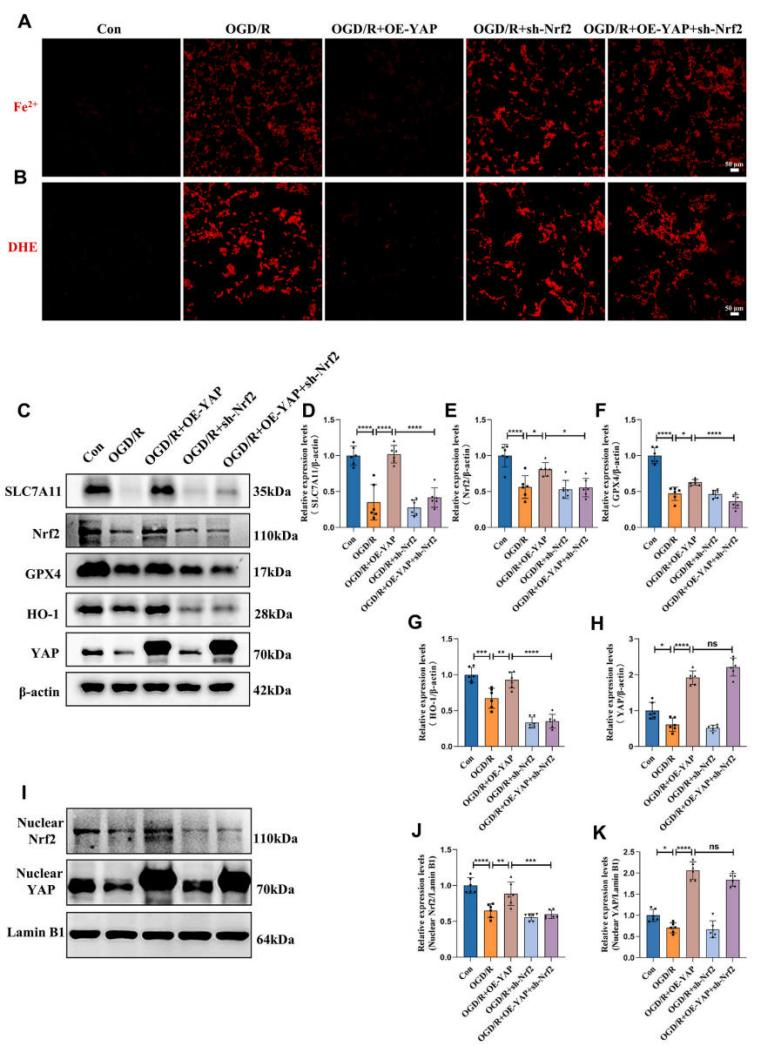
YAP作为转录共激活因子,主要通过与TEAD转录因子相互作用发挥转录调控功能[30]。为探究YAP对Nrf2的潜在转录调控作用,研究团队利用JASPAR数据库预测Nrf2启动子区域内的TEAD转录因子结合位点。分析结果显示Nrf2启动子区可能存在YAP/TEAD相关结合序列:AAATTCC、TCATACCT和ACATTTCA。然而ChIP-PCR实验表明YAP并未通过TEAD与Nrf2启动子结合。为进一步验证YAP是否能转录调控Nrf2,进行荧光素酶报告实验,结果显示Nrf2启动子活性未显著增加。这些结果表明YAP并不直接转录激活Nrf2表达。随后,进一步研究了YAP是否可能通过直接相互作用在蛋白质水平调控Nrf2。共免疫沉淀(Co-IP)分析显示,YAP与Nrf2蛋白存在直接结合。因此,研究结果表明:YAP可能通过与Nrf2蛋白结合并促进其核转位来发挥抗铁死亡和肺保护作用,而非通过激活Nrf2的转录表达来调控下游靶基因。
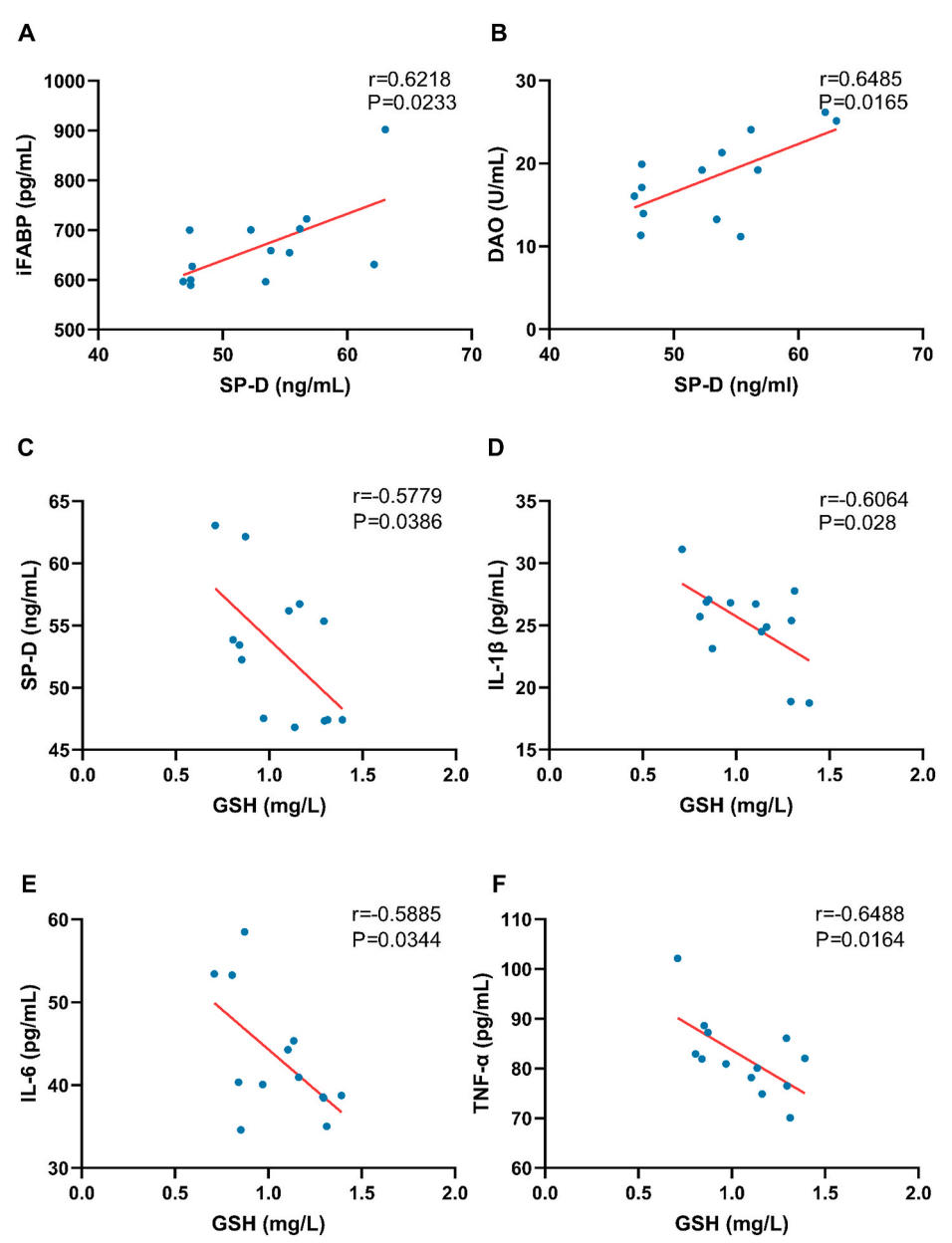
为探究接受体外循环患者的肺损伤与铁死亡之间的关联,本研究对体外循环术后6小时的患者血液样本进行线性相关性分析。结果显示SP-D与胃肠道损伤和肠屏障功能障碍的标志物:肠道脂肪酸结合蛋白(iFABP)及二胺氧化酶(DAO)呈正相关,而谷胱甘肽(GSH)则与SP-D、TNF-α、IL-6和IL-1β呈负相关。这些发现表明,体外循环诱导的肠道缺血再灌注损伤可能与铁死亡有关。
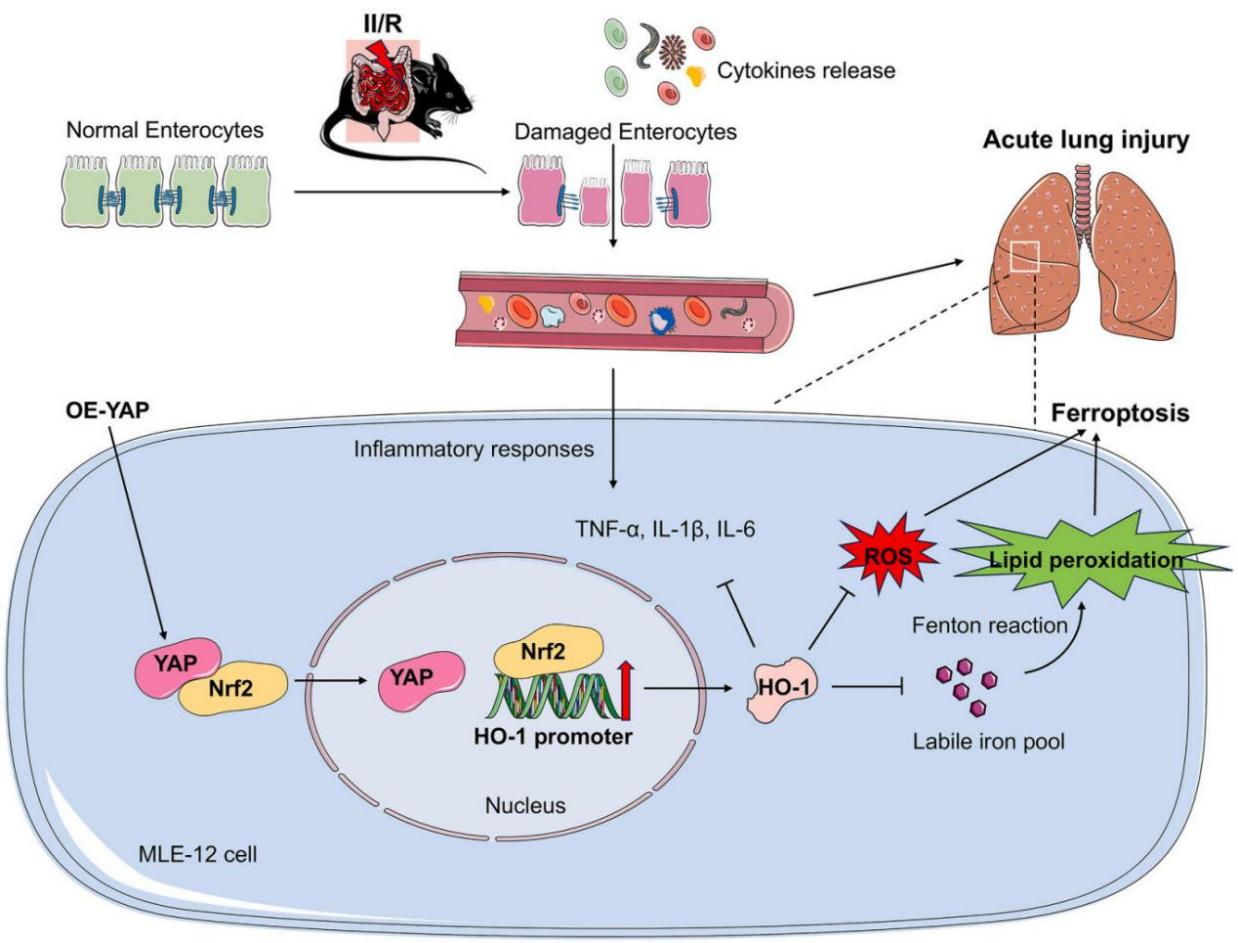
本研究结果表明,铁死亡和YAP在II/R诱导的急性肺损伤(ALI)病理生理机制中起重要作用。YAP在细胞核内表达量的增加有助于抵抗铁死亡,并通过与Nrf2结合促进其核转位来缓解ALI。